Željezo
| Željezo | ||
|---|---|---|
|
| ||
| Osnovna svojstva | ||
Element Simbol Atomski broj |
Željezo Fe 26 | |
| Kemijska skupina | prijelazni metali | |
| Grupa, perioda, Blok | 8, 4, d | |
| Izgled | sivkasta krutina
| |
| Gustoća1 | 7874 kg/m3 | |
| Tvrdoća | 608 MPa (HV), 490 MPa (HB), 4,0 (Mohsova skala) | |
| Specifični toplinski kapacitet (cp ili cV)2 |
(25 °C) 25,10 J mol–1 K–1 | |
| Talište | 1538 °C | |
| Vrelište3 | 2862 °C | |
| Toplina taljenja | 13,81 kJ mol-1 | |
| Toplina isparavanja | 340 kJ mol-1 | |
|
1 pri standardnom tlaku i temperaturi | ||
| Atomska svojstva | ||
| Atomska masa | 55,845(2) | |
| Elektronska konfiguracija | [Ar] 3d6 4s2 | |
Željezo je kemijski element atomskog (rednog) broja 26 i atomske mase 55,845(2) . U periodnom sustavu elemenata predstavlja ga simbol Fe.


Simbol Fe dolazi od ferrum, latinskog naziva za željezo. Ferat je naziv za željezo u anionskom kompleksu. Telursko željezo je naziv za elementarno željezo, koje je nastalo u Zemljinoj kori. Željezo ima četiri stabilna izotopa (maseni brojevi 54, 56, 57 i 58), od kojih je najobilniji 56Fe (91,72%), te s više nestabilnih, radioaktivnih izotopa (najstabilniji je 60Fe). Željeza ima u meteoritima (metalni meteoriti), na Mjesecu, spektralnom analizom ustanovljena je njegova zastupljenost i na Suncu. Na Zemlji je vrlo rašireno, ali je u elementarnom stanju rijetko, jer se lako spaja s kisikom i drugim nemetalima. Pretpostavlja se da se najdublja unutrašnjost Zemlje također sastoji od željeza.
Željezo, kad je potpuno čisto, srebrnkastog je sjaja i mekano. Poznato je od pradavnih vremena, a danas sigurno najvažniji tehnički metal koji se upotrebljava na mnogo načina. Najvažnije je od svih metala i uglavnom se koristi kao čelik, u kojem ima ugljika (do 2,06%). Željezo hrđa na vlažnom zraku i otapa se u razrijeđenim kiselinama. Željezo je prijelazni metal 8. skupine periodnog sustava elemenata.
Željezo u prirodi najčešće dolazi kao mineral magnetit. Kristalizira u obliku crnih kubičnih kristala. U građi Zemljine kore željezo je najzastupljeniji metal, a među elementima se s udjelom od približno 5,63% nalazi na četvrtom mjestu (iza kisika, silicija i aluminija). Željezo vezano u spojevima može se naći u približno 400 minerala, od kojih su najpoznatiji hematit (udjel željeza 70,0%), magnetit (71,4%), limonit (do 62%), pirotin (62%), siderit (48,2%), pirit (46,5%). Karakteristična žuta, smeđa ili crvena boja zemlje potječe upravo od željeznih spojeva. Za tehničko dobivanje željeza isplativa je preradba ruda koje sadrže više od 25% željeza, a najcjenjenije su oksidni i karbonatni rudni minerali s približno 50 do 60% željeza, što su praktički samo hematit, magnetit, limonit i donekle siderit.[1] Koncentracija željeza u morima je vrlo mala (oko 4x10−3 ppm). Elementarno željezo se u prirodi nalazi samo kao meteorno, dospjelo na zemlju iz svemira i telurno prisutno u Zemljinoj kori od iskonskih vremena. Prisutnost željeza utvrđena je i u sastavu Sunca, Mjesečevim stijenama i drugim nebeskim tijelima gdje ga ima oko 14,3%, kako svjedoče meteoriti pali na Zemlju od kojih se polovina sastoji pretežno od željeza. Na površini Zemlje prirodno željezo je samo izuzetno u elementarnom stanju (telurno željezo na otoku Disko, zapadno od Grenlanda).
Svojstva
Elementarno željezo u čistom je stanju poput srebra bijel, razmjerno mekan, kovak metal s talištem 1 538 °C i gustoćom 7 874 kg/m³, kemijski dosta otporan. Njegova toplinska i električna provodnost iznosi samo petinu do šestinu provodnosti bakra. Također, ono je i feromagnetično, što znači da zadržava magnetska svojstva i prestankom djelovanja magnetskog polja. Željezo je kemijski vrlo reaktivno i kao neplemeniti metal otapa se u neoksidirajućim kiselinama. Na zraku je vrlo nestabilno i relativno brzo oksidira (korozija). U oksidirajućim kiselinama (koncentriranoj sumpornoj i dušičnoj kiselini) površina željeza se ne otapa, nego pasivizira stvaranjem zaštitnog sloja.
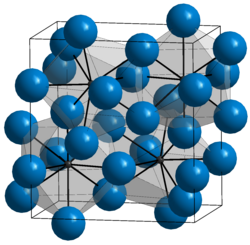
Kristalna struktura željeza se mijenja s promjenom temperature. Čisto elementarno željezo (Fe°) ima 3 kristalne forme (alotropske modifikacije):
- alfa-željezo (α-Fe) ili ferit, stabilno na sobnoj temperaturi ispod 906 °C s prostorno centriranom kockom, magnetično je, a u čvrstom stanju može otopiti vrlo malo ugljika, feromagnetično je, a na temperaturi od 768 °C postaje paramagnetično;
- gama-željezo (γ-Fe) ili austenit, stabilno između 906 i 1403 °C s nemagnetičnom plošno centriranom kockom; nemagnetično je i u čvrstom stanju može otopiti mnogo ugljika;
- delta-željezo (δ-Fe) stabilno iznad 1403 °C s prostorno centriranom kockom.[2]
Alfa-željezo je feromagnetično do Curiejeve temperature od 770 °C (1043 K). Pri temperaturi 770 °C gubi feromagnetska svojstva, ali ne mijenja strukturu, pa se ponekad pogrešno naziva i beta-željezo. Na svojstva željeza znatno utječe već i malen udjel primjesa ili nečistoća. Tako je na primjer talište željeza koje sadrži 0,83% ugljika (eutektički sastav ili perlit) gotovo 800 °C niže od tališta čistoga željeza.
Željezo ima 9 izotopa (maseni broj od 52 do 60) i četvrti je element po udjelu u zemljinoj kori. U prirodi se željezo nalazi kao smjesa četiri stabilna izotopa: 54Fe (5,8%), 56Fe (91,72%), 57Fe (2,2%) i 58Fe (0,28%), a ostali su izotopi radioaktivni, s kratkim vremenom poluraspada, osim izotopa 60Fe (t1/2 = 3x105 godina). Izotop 56Fe poznat je kao nuklid s najstabilnijom atomskom jezgrom, jer ima najveću nuklearnu energiju vezanja.
Željezo se otapa u razrijeđenim kiselinama, u kiselinama s neoksidirajućim djelovanjem (na primjer u solnoj) te u vrućoj koncentriranoj natrijevoj lužini. Međutim, ne otapa se i ne nagrizaju ga koncentrirane kiseline s oksidirajućim djelovanjem (sumporna i dušična), jer u njima željezo postaje pasivno stvaranjem površinskoga oksidnog sloja (pasivnost metala). Željezo je na suhom zraku stabilno, ali na vlažnom zraku i u vodi korodira stvaranjem hrđe na svojoj površini, koja je po kemijskom sastavu hidratirani željezni(III) oksid (FeOOH). Sloj je hrđe porozan, mekan i lako se ljušti, ne štiti površinu željeza od daljnje korozije, pa je zbog toga korozija željeza velik tehnički problem. Sitnije čestice željeza mogu na zraku gorjeti, a u sasvim finom razdjeljenju željezo je piroforno, to jest samozapaljivo na zraku. Pri umjerenim temperaturama željezo se spaja u binarne spojeve s mnogim nemetalima, ponajprije s kisikom, ali i sa sumporom, ugljikom, halogenim elementima, arsenom, fosforom i silicijem te s nekim plinovima (amonijak, ugljikov dioksid) i vodenom parom.
Kao biogeni element, željezo spada u grupu esencijalnih elemenata gdje sudjeluje u prijenosu kisika. Željezo je važno za život biljaka i životinja i nalazi se u sastavu hemoglobina i kloroplasta u krvi, pa ga mora sadržavati hrana toplokrvnih životinja, kao i zemlja u kojoj rastu biljke. U organizmu odraslog čovjeka ima oko 5,85 grama željeza; od toga je 55% vezano za hemoglobin, 10% ga je u mioglobinu i 17% u staničnim heminima; oko 17% željeza nalazi se i u drugim organima (kao feritin i hemosiderin). Preparati željeza ubrajaju se u najstarija ljekovita sredstva; bili su poznati već u rimsko vrijeme. Danas se željezo u obliku topljivih ferosoli najviše upotrebljava za liječenje raznih oblika anemija. Manjak željeza dovodi do anemije, a višak može izazvati oštećenje jetre i bubrega. Za neke spojeve željeza se sumnja da su kancerogeni.[3]
Željezne slitine
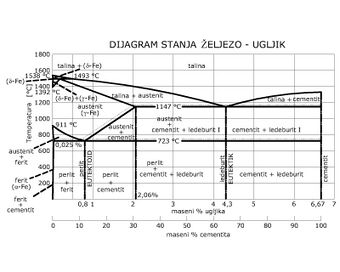
Različite vrste tehničkoga željeza, koje se koriste kao tehnički, konstrukcijski materijal, zapravo su slitine željeza s ugljikom. Dvije su vrste takvih slitina: čelik i lijevano željezo. Rastaljeno željezo može otopiti do 6,67% ugljika, dok je topljivost ugljika u čvrstom željezu mnogo manja, pa se višak ugljika izlučuje kao željezov karbid, Fe3C (cementit) ili, pri ekstremno polaganom hlađenju, kao grafit. Poznato je više faza i strukturnih oblika željeznih slitina različita sastava; osnovni su strukturni oblici ferit, austenit i cementit, a njihove su smjese perlit i ledeburit. Njihovo ravnotežno stanje na određenoj temperaturi prikazuje dijagram stanja željezo–ugljik. Taj je dijagram temelj za tumačenje razlika među svojstvima različitih slitina željeza s ugljikom, ili iste slitine tih elemenata na različitim temperaturama odnosno, za tumačenje promjena koje nastaju u tim slitinama kada se podvrgavaju obradbi pri kojoj im se mijenja temperatura ili sastav, ili oboje istodobno. Dijagram prikazuje odnose termodinamičke ravnoteže u dvama binarnim sustavima. Pune linije prikazuju granice između faza u metastabilnom sustavu Fe-Fe3C, a isprekidane linije u stabilnom sustavu Fe-C. Iznad linije ABCD (odnosno ABC′D′), zvane likvidus, slitina se nalazi u rastaljenom stanju (talina), a ispod linije AGHECF (odnosno AGHE′C′F′), zvane solidus, slitina je u čvrstom stanju. Linija likvidus pokazuje na kojim se temperaturama pri hlađenju taline određenoga sastava počinju izlučivati kristali, odnosno na kojoj će se temperaturi pri zagrijavanju slitine određenoga sastava rastaliti i posljednji kristalić, a linija solidus pokazuje na kojim temperaturama očvrsne i posljednja kap pri hlađenju taline, odnosno počinje se taliti slitina određenoga sastava. Slitina se u temperaturnom području između tih dviju linija sastoji od različitih smjesa preostale taline, α-željeza, δ–željeza i cementita. Ostale linije na dijagramu prikazuju ovisnost temperature prijelaza jedne čvrste faze u drugu o udjelu ugljika, uz pretpostavku da se temperaturne promjene odvijaju dovoljno polagano.
Od željeznih slitina koje ne sadrže ugljik važne su feroslitine (ferolegure). One uz željezo sadrže i velik, često i pretežan udjel drugih metala, ali se od njih ne izrađuju konačni proizvodi, nego one služe za dodavanje drugih elemenata u taline čelika i lijevanoga željeza radi legiranja, a i za uklanjanje nepoželjnih sastojaka iz talina.
Kemijski spojevi željeza
| Oksidacijska stanja |
Predstavnici kemijskih spojeva |
|---|---|
| −2 | rijetki - Na2[Fe(CO)4]; atomska ljuska d10 |
| −1 | rijetki – [Fe2(CO)8]2; atomska ljuska d9 |
| 0 | [Fe(CO)5]; atomska ljuska d8 |
| 1 | rijetki – Na2[Fe(NO)(OH2)5]; atomska ljuska d7 |
| 2 (dvovalentno željezo) |
FeO, FeS2, Fe(OH)2, [Fe(OH2)6]2 + (voda), FeF2, [Fe(η-C5H5)2] itd.; atomska ljuska d6 |
| 3 (trovalentno željezo) |
Fe2O3, Fe3O4, FeF3, FeCl3, Fe(OH)(O), [Fe(OH2)6]3+ (voda) itd.; atomska ljuska d5 |
| 4 | rijetko, neki kompleksi; atomska ljuska d4 |
| 5 | [FeO4]3 (?); atomska ljuska d3 |
| 6 | K2[FeO4]; atomska ljuska d2 |







Među najvažnije željezne spojeve ubrajaju se oni s oksidacijskim brojem II i III, dvovalentno ili trovalentno željezo (prije zvani fero-spojevi, odnosnog feri-spojevi). Željezo pravi spojeve u kojima ima oksidacijski broj +2, +3 i +6, a u najvažnijima i najvećem broju spojeva ima oksidacijski broj +2 (fero) i +3 (feri). Stanje +2 je najstabilnije. Šesterovalentno željezo je ferat ion FeO4 - koji je postojan samo u lužnatom mediju, a u kiselom mediju se raspada na Fe3+ i kisik, uz nešto ozona.[4] Nestabilniji Fe2+ ion u vodenoj se otopini u prisustvu kisika lako oksidira u Fe3+ ion. Željezo zbog svog negativnog standardnog elektrodnog potencijala Fe2+/Fe otapa se u kiselinama uz razvijanje vodika. Ioni Fe2+ i Fe3+ imaju izraženu sposobnost stvaranja kompleksa koordinacijskog broja 6. Otopina iona Fe2+ je svijetlo zelene boje. Otopina iona Fe3+ je žute boje, osim bromida koji je crvene. Dimetil-glioksim oboji otopinu Fe2+ iona u crveno.[5]
Željezovi spojevi s kisikom
Od željezovih oksida važni su:
- željezov(III) oksid (Fe2O3) i fero-feri-oksid (Fe3O4 · Fe2O3), koji nastaje kao crveni prah kad se žari Fe(OH)3, Fe(NO3)2 ili Fe2(SO4)3. Kao mineral, hematit tvori više ili manje guste stijene, mjestimice i velike crvene kristale, i najvažniji je rudni mineral za dobivanje željeza. Koristi se i kao sredstvo za poliranje i za pročišćavanje plinova, kao crveni pigment (caput mortuum, kolkotar, oker) i katalizator;
- željezov(II, III) oksid (FeO · Fe2O3 = Fe3O4) ili feri-fero-oksid je crni prah, nastaje pri žarenju željeza i željeznih oksida na višim temperaturama, ali je i rudni mineral magnetit (najvažnija ruda ili mineralna sirovina)), služi kao crni pigment i elektrodni materijal, sastojak je termitne smjese. Miješani oksidi nekoga dvovalentnog metala i željeza(III) poznati su pod nazivom feriti kao elektrokeramički tehnički materijali;
- željezov(II) hidroksid, Fe(OH)2, ispada kao bijeli do svijetlozeleni talog kad se otopini soli dvovalentnog željeza u odsutnosti kisika doda lužina. Na zraku lako prelazi u smeđecrveni, amorfni željezov(III) hidroksid, Fe(OH)3, a zapravo je željezni oksidhidrat, Fe2O3 · x H2O. Taj se taloži (s promjenjivim količinama apsorbirane vode) kao crvenosmeđi hladetinasti talog, kad se otopini soli trovalentnog željeza doda lužina. Sastojina je različitih minerala i stijena (hidrohematit, turgit, limonit, ksantosiderit, getit, stilpnosiderit, oker, lepidokrokit).
Željezovi spojevi s dušikom
Od željezovih nitrata važni su:
- željezov(II) nitrat (Fe(NO3)2) nastaje kada se željezo otapa u razrijeđenoj dušičnoj kiselini koja je potrebno da bude vruća. Hladna koncentrirana HNO3 ne otapa željezo jer na površini nastaje zaštitni sloj oksida. Kristalizira iz otopine sa 6 ili 9 molekula (Fe(NO3)2 i Fe(NO3)3) vode u bezbojnim kristalima koji se otapaju u vodi i zbog hidrolize daju smeđu otopinu. Upotrebljava se u medicini kao adstringens protiv krvarenja u želucu i crijevima. Također služi za otežavanje svile, za štavljenje kože, kao močilo u bojadisarstu i bojadisarskom tisku, za proizvodnju berlinskog modrila i drugo. Željezov(II) nitrat otopljen u vodi otopina poprimi zelenu boju;
- željezov(III) nitrat željezova je sol kemijske formule Fe(NO3)3. Budući je higroskopan, često se nalazi u nonahidratnom obliku, Fe(NO3)3 x 9H2O), koji je kristalna tvar bezbojne do blijedo ljubičaste boje. Nastaje reakcijom željeza ili željezovih oksida s dušičnom kiselinom.
Željezovi spojevi s ugljikom
Od željezovih karbida i karbonata važni su:
- željezov karbid ili cementit (F3C) je vrlo tvrd i krt spoj, sastojina je tehničkog željeza koja uzrokuje njegovu tvrdoću;
- željezov(II) karbonat (FeCO3, siderit) je poznata karbonatna ruda željeza, nalazi se u prirodi kao mineral siderit. Nastaje kao bijel amorfan talog kad se otopina soli dvovalentnog željeza (bilo koje željezove(II) soli) pomiješa s otopinom sode bikarbone. Na zraku gubi ugljikov dioksid i oksidira se na Fe2O3. U vodi ima topljivost 3,13 x 10−11. U vodi koja sadrži otopljeni ugljikov dioksid polako se otapa u obliku hidrokarbonata (Fe(HCO3)2), sastojaka mnogih temeljnih i mineralnih voda. Tako nastaju mineralne vode (voda koja sadržava ugljikov dioksid), željezovite kiselice. Iz njih se u dodiru sa zrakom taloži smeđi oksidihidrat, pa stoga prirodne vode s mnogo željeza nisu prikladne za piće i u industrijske svrhe.
Željezovi spojevi s halogenim elementima
Željezovi(II) halogenidi su FeBr2, FeF2, FeI2 i FeCl2 i svi su topljive soli, dok su željezovi(III) halogenidi FeF3, FeCl3 i FeBr3, od kojih je željezov(III) fluorid neznato topljiv:
- željezov(II) klorid (FeCl2 x 4H2O) tvori modrozelene monoklinske kristale koji se na zraku raskvasuju i topljivi su u vodi; dobiva se otapanjem željeza u klorovodičnoj kiselini ili direktnom sintezom iz elemenata. Služi kao reducens u proizvodnji bojila, kao sredstvo za reduciranje. Iskristalizira kao hidrat iz otopine dobivene otapanjem željeza u solnoj kiselini. Razrijeđena otopina je žuta, a koncentriranije budu crvene. Bezvodni se dobije grijanjem željeza u atmosferi klorovodika. Dobiva se otapanjem željeza u klorovodičnoj kiselini ili direktnom sintezom iz elemenata. Željezo na zraku brzo zahrđa jer je vlažno i puno elektrolita. Otud zelena boja željezovim(II) solima, osim hidroksida i sulfida.
- željezov(III) klorid heksahidrat (ili tetrahidrat, FeCl3 x 6 H2O). Hidratiziran je žute boje. Na zraku se raskvasuje, pa je lako topljiv u vodi, alkoholu i eteru. Rabi se kao kemijski reagens, kao koagulans u čišćenju površinskih voda, oksidacijsko i kondenzacijsko sredstvo, kao prenosilac klora u sintezi bojila, močilo u bojadisarstvu pri bojenju tekstila, za nagrizanje metala (izradba tiskanih pločica u elektrotehnici), u medicini kao adstrigens (vata za zaustavljanje krvarenja rana), i tako dalje. Dolazi u trgovinu u obliku prljavožutih kristalnih gruda (obično kao heksahidrat - sa 6 molekula vode). Bezvodni klorid je higroskopna tvar. Nastaje žarenjem željeza u struji suhog klora ili otapanjem željeza u klorovodičnoj kiselini uz uvođenje klora. Kristalizira iz vodene otopine dobivene otapanjem željezovog(III) oksida u solnoj kiselini.
Željezovi spojevi sa sumporom
Od željezovih sulfida i sulfata važni su:
- željezo(II) sulfid (FeS) u prirodi dolazi kao mineral pirotin (brončane boje), dobiva se u obliku tamnosivih ili crnih gruda, ploča ili štapića s metalnim sjajem time što se rastavljena smjesa željeza i sumpora lijeva na odgovarajuću površinu ili u kalup; u razrijeđenim kiselinama otapa se uz razvijanje sumporovodika H2S, pa se u laboratoriju upotrebljava za dobivanje toga plina. Sulfid ion (S2-) taloži crni talog u neutralnoj otopini, koji nije topljiv u vodi, ali je topljiv u kiselinama:
- Fe2+ + S2- → FeS
- FeS + 2 H+ → Fe2+ + H2S
- željezov disulfid (FeS2) poznata je sulfidna ruda željeza i vrlo je raširen u prirodi kao mineral pirit (manje kao markazit) koji je zlatnožute boje s metalnim sjajem. Iz njega se prženjem dobiva sumporov dioksid za proizvodnju sulfita (time i sumporaste kiseline) i sulfatne kiseline. Sumporovodik u kiseloj otopini reducira željezo uz izlučivanje sumpora:
- 2 Fe3+ + H2S ⇌ 2 Fe2+ + S2H+
- Amonijev sulfid ((NH4)2S) taloži crni talog koji je topljiv u kiselini:
- 2 Fe3+ + 3S2- ⇌ Fe2S3
- Fe2S3 + 6 HCl --> 2 FeCl3 + 3 H2S
- željezov(II) sulfat (FeSO4 x 7H2O) ili zelena galica dobiva se u obliku svijetlozelenih monoklinih prizama iz otopine željeza u sumpornoj kiselini; u tehnici se dobiva i oksidacijom pirita na vlažnom zraku, a otpada u znatnim količinama kao sporedni proizvod pri cementaciji bakra, pri dobivanju kositra, pri proizvodnji krom alauna i titanskog bjelila; najvažnija je tehnička željezna sol i služi za dobivanje drugih spojeva željeza, također za proizvodnju tinte, za uništavanje štetnika (insekticid) i korova, u bojadisarstvu i kožarstvu, za dezinfekciju i dezodorizaciju, za konzerviranje drveta, u veterinarskoj medicini kao adstringens, kao flokulant ili bistrilo u čišćenju vode i tako dalje;
- željezov(III) sulfat (Fe2(SO4)3) tvori bijeli ili sivobijeli prah koji se u vodi polako topi, a na zraku se raskvasuje dajući smeđu tekućinu; dobiva se tako da se kisela otopina zelene galice oksidira dušičnom kiselinom; služi kao močilo u bojadisarstu, u proizvodnji berlinskog modrila i željeznih alauna, koji se upotrebljavaju u bojadisarstvu, fotografiji i kemijskoj analizi;
- amonijev željezov(II) sulfat heksahidrat (NH4)2Fe(SO4) x 36H2O poznat je kao Mohrova sol.
Organski željezovi spojevi
Od organskih željezovih spojeva važni su:
- željezov(II) acetat, (CH3COO)2Fe x 4H2O ili Fe(C2H3O2)2 ili Fe(CH3COO)2) dobiva se otapanjem željeza u octenoj kiselini, a upotrebljava se u bojadisarstvu kao močilo i u medicini kao adstringens:
- 2CH3COOH + Fe → (CH3COO)2 Fe + H2
- željezov(III) acetat (Fe(CH3COO)3) u vodi tvori crveni talog. Inače tako se općenito dokazuje Fe2O3 (→ 6CH3COOH + 2Fe → 2(CH3COO)3Fe + 3H2);
- željezov amonijev oksalat, (NH4)3Fe(C2O4) x 3H2O, zeleni, u vodi lako topljivi kristali koji na svjetlu gube oksalnu kiselinu oksidacijom na CO2, pri čemu trovalentno željezo prelazi u dvovalentno. To se svojstvo upotrebljava za mjerenje količine svjetla i za kopiranje nacrta i slično. U istu svrhu, a i kao lijek protiv slabokrvnosti, upotrebljava se i željezov(II) citrat.
Složeni spojevi željeza
Željezo gradi mnoge složene spojeve, od kojih su među najstabilnijima cijano-kompleksi:
- kalijev heksacijanoferat(II) trihidrat, K4[Fe(CN)6] · 3H2O ili žuta krvna sol, industrijska je kemikalija (bojenje tkanina, elektroplatiranje, graviranje, litografija, kemijska analiza). Oksidacijom kisikom iz zraka nastaje berlinsko modrilo, Fe4[Fe(CN)6]3, poznat željezni pigment. Ako se u njem jedna cijanidna skupina zamijeni drugim ligandom, na primjer s H2O ili NH3, nastaju prusijati;
- kalijev heksacijanoferat(III), K3[Fe(CN)6] ili crvena krvna sol, koristi se za štavljenje kože, proizvodnju pigmenata i kao katalizator. Od njega se odvodi plavi pigment Turnbullovo modrilo, sastava identičnoga berlinskomu modrilu;
- s ugljikovim monoksidom željezo tvori karbonilne komplekse, među kojima je najpoznatiji pentakarbonilželjezo(0), Fe(CO)5; na njegovu se raspadu temelji jedan od postupaka dobivanja čistoga željeza;
- poznat je i ferocen (diciklopentadienil-željezo), (C5H5)2Fe, organometalni kompleksni spoj željeza s takozvanom strukturom sendviča, vrlo djelotvoran katalizator reakcija polimerizacije.
Upotreba











Željezo je najkorišteniji od svih metala i njegova proizvodnja čini 95% (maseno) od ukupne svjetske proizvodnje metala. Razlog tome je kombinacija niske cijene i pogodnih fizičkih svojstava, zbog čega je željezo neizostavni materijal u automobilskoj industriji, brodogradnji i graditeljstvu.
Tehničko željezo predstavlja redovito leguru željeza s većim ili manjim količinama ugljika, silicija, mangana, sumpora i fosfora, pa mu svojstva uvelike ovise o količini tih sastojina, odnosno primjesa. Dodacima drugih metala, kao kroma, titanija, molibdena, nikla, tantala, vanadija, kobalta, niobija, volframa i drugog, svojstva željeza se mogu i dalje mijenjati u širim granicama nego bilo kojeg drugog tehničkog metala. Stoga danas ima na tisuće vrsta tehničkih željeza za najrazličitije namjene. Tehničko željezo, osim vrsta koje su posebnim dodacima (napose nikla i kroma) učinjene kemijski otpornima (nehrđajući čelik), kemijski je manje otporno nego čisto. Ono na vlažnom zraku hrđa, to jest prevlači se slojem hidroksida koji ne štiti metal od daljeg nagrizanja. Željezo grijano na višu temperaturu pokriva se crvenom prevlakom oksida Fe3O4.
Željezo je čovjeku bilo poznato već u prapovijesno doba, u kojem je obilježilo jedno cijelo tehnološko i kulturno razdoblje (željezno doba). Od davnine do danas ono je u obliku čelika najvažniji tehnički materijal, bez kojega je suvremena civilizacija nezamisliva. Od kemijskih elemenata, izuzevši kisik, najviše se u elementarnom obliku koristi željezo, jer je rašireno, lako se dobiva i prerađuje i ima poželjna mehanička i uporabna svojstva. Od njega se izrađuju golemi proizvodi kao što su najrazličitiji strojevi, vozila, brodovi, mostovi i građevine, ali i bezbrojni manji predmeti potrebni u svakodnevnom životu. Željezo je vrlo važno i za život biljaka i životinja, pa ga mora sadržavati hrana toplokrvnih životinja i zemlja u kojoj rastu biljke. Nalazi se u svim živim stanicama: sastojak je hemoglobina, koji je bitan u procesu disanja, te mioglobina, u kojem se kisik privremeno pohranjuje u mišićima za daljnje potrebe staničnoga disanja, zatim služi kao oksidans u enzimima, sudjeluje u vezanju atmosferskoga dušika i drugo. U organizmu se nakuplja u bjelančevini feritinu u jetri, slezeni i koštanoj srži, odakle se po potrebi može brzo mobilizirati. Biljke uzimaju željezo iz tla u obliku njegovih u vodi topljivih spojeva, ioni Fe2+ oksidiraju se u ione Fe3+, a oni tvore kelatne komplekse, pa se željezo u tom obliku prenosi u zelene dijelove biljaka. Preparati željeza ubrajaju se u najstarija ljekovita sredstva i bili su poznati već u rimsko doba. Danas se željezo u obliku topljivih spojeva primjenjuje u liječenju anemije.
Kemijski čisto željezo
Kemijski čisto željezo proizvodi se rijetko jer su mu, u usporedbi s čelikom, fizikalna i mehanička svojstva slabija, proizvodni postupci složeniji, pa i troškovi veći, a upotreba ograničena samo na područje metalurgije praha, katalizu te proizvodnju specijalnih magneta. Tehnički čisto (99,5 do 99,9% Fe) i čisto željezo (99,90 do 99,99% Fe) dobiva se redukcijom čistoga željeznog oksida ili hidroksida vodikom pri 700 °C, raspadom pentakarbonilželjeza pri 250 °C ili elektrolizom nekih željeznih spojeva, a vrlo čisto željezo (više od 99,99% Fe) zonskim taljenjem čistoga karbonilnog ili elektrolitičkoga željeza.
Tehničko željezo
Tehničko željezo, to jest različite vrste željeza koje se koriste kao tehnički, konstrukcijski materijal, dobiva se ponajprije redukcijom rudnih minerala ugljikom iz koksa u visokoj peći. Tako nastaje sirovo željezo, koje obično sadrži 3,5 do 4,5% ugljika, 0,5 do 3,5% silicija, 0,5 do 6% mangana, 0,1 do 2% fosfora i 0,01 do 0,05% sumpora. Zbog velikog udjela ugljika sirovo željezo vrlo je krhko i ne može se plastično deformirati, a u proizvode se može izravno oblikovati jedino lijevanjem (lijevano željezo). U te se svrhe troši samo manji dio proizvedenoga sirovog željeza, dok se njegova glavnina prerađuje u čelik. Redukcijom u visokoj peći proizvodi se 95% tehničkog željeza. Ostatak se proizvodi drugim postupcima, koji su rezultat nastojanja da se izbjegne primjena visokokvalitetnoga metalurškoga koksa, nužnoga za proces u visokoj peći. To je posebno važno za zemlje koje nemaju vlastitih nalazišta ugljena prikladnoga za proizvodnju metalurškoga koksa, a imaju drugih vrsta ugljena ili jeftine izvore električne energije. Osim redukcijom u električnim pećima (u kojima je izvor topline električni luk) te procesom u kojem se redukcija povezuje s isplinjavanjem ugljena, željezo se u tim zemljama dobiva i izravnim redukcijskim procesom, koji se sastoji u redukciji oksidnih ruda u obliku peleta u niskim jamskim ili rotacijskim pećima na temperaturama između 750 i 1050 °C. Reducensi su obično plinoviti (ugljikov monoksid, vodik ili njihova smjesa), a rjeđe ugljen proizvoljne kvalitete i krupnoće. Tako nastaje takozvano spužvasto željezo, čvrst proizvod velike poroznosti, koji se daljnjom obradbom u elektrolučnim pećima može preraditi u kvalitetan čelik. Prije poznavanja proizvodnje u visokoj peći, proizvodilo se samo spužvasto željezo.
Željezna je ruda po količini na drugom mjestu među robom kojom se u svijetu najviše trguje. Njezina najveća ležišta nalaze se u Brazilu i Australiji. Te su zemlje ujedno i najveći ponuđači željezne rude na svjetskom tržištu, a glavni je uvoznik Japan. Godine 2007. u svijetu je iskopano 1,9 · 109 tona željezne rude, a proizvedeno je 946 · 106 tona sirovoga željeza (Kina 469,5 · 106 tona, Japan 86,8 · 106 tona, Rusija 51 · 106 tona, SAD 36,2 · 106 tona, Ukrajina 35,6 · 106 tona, Brazil 35,5 · 106 tona, Njemačka 31,2 · 106 tona, i tako dalje) te 55 · 106 tona spužvastoga željeza.
Čelik
Primjena željeza je prvenstveno u obliku čelika, a manje kao sirovog ili lijevanog željeza. Čelik je legura željeza s 0,05 do 2,06% ugljika. To je najvažniji tehnološki i konstrukcijski materijal, a do danas je poznato više od tisuću vrsta čelika. Odlikuju se velikom čvrstoćom, tvrdoćom, žilavošću, mogućnošću lijevanja i mehaničke obrade, te velikom elastičnošću.
Lijevano željezo
Lijevano željezo ili željezni lijev je legura željeza i ugljika, te nekih drugih legirnih elemenata, gdje je sadržaj ugljika veći od 2,06% (maseni udio). Za razliku od lijevanog željeza, čelik je legura željeza i ugljika, s manje od 2,06 % ugljika, uz prisutne pratioce (silicij, mangan) i nečistoće (fosfor, sumpor i druge) i eventualni dodatak jednog ili više legirnih elemenata. U praksi se pod lijevanim željezom obično podrazumijeva sivi lijev, koji se najviše primjenjuje. Lijevano željezo dobiva se lijevanjem sirovog željeza u visokim pećima. Sadržaj ugljika je kod lijevanog željeza obično između 2,5 i 3,5%. Struktura lijevanog željeza može biti feritna, feritno–perlitna i perlitna, zbog čega je sivom lijevu čvrstoća u rasponu od 100 N/mm2 za feritnu strukturu, do 400 N/mm2 za perlitnu strukturu, te od 380 do 700 N/mm2 kod žilavog lijeva (nodularni lijev).
Povijest
Arheološki dokazi upotrebe meteoritskog željeza za izradu sitnog nakita i oružja sežu do 5. tisućljeća pr.Kr., u današnjem Iranu i vrhovi koplja, koji datiraju iz 4. tisućljeća pr.Kr. iz drevnog Egipta. Zapisi hijeroglifima iz 2. stoljeća pr.Kr. govore o "crvenom balonu s neba", što se odnosi na meteoritsko željezo. Ovo se je željezo koristilo kao ukrasni dio na vrhovima koplja. To željezo ljudi tada nisu dobivali lijevanjem ili taljenjem željeznih ruda, nego su ga obrađivali kao što su obrađivali kamen.
Negdje između 3. i 2. tisućljeća pr. Kr. pronalaze se ostaci obrađenog željeza u području Mezopotamije, Anatolije i Egipta. Ovakvi rani počeci obrađenog željeza razlikuju se od željeza meteoritskog porijekla, jer ne sadrže nikal u svom sastavu. Čini se da su ljudi tada ovo željezo koristili isključivo u religijske svrhe, a željezo je tada bilo vrijednije od zlata i vjerojatno je nastalo kao višak kod proizvodnje bronce.
Između 16. i 12. stoljeća pr. Kr. željezo se počinje snažnije koristiti; doduše i u to vrijeme bronca je se još uvijek snažno koristila. No od 1 200. pr. Kr. počinje prijelaz brončanog doba u željezno doba. Smatra se da ovaj prijelaz ljudskog društva nije potaknula premoć i kvaliteta jednog materijala nad drugim, nego nedostatak kositra (koji je naime neophodan za dobivanje bronce). Ovi prvi koraci obrade željeza na počecima željeznog doba uključivali su i korištenje drvenog ugljena tijekom obrade, a rezultat ovakve obrade željeza bio je prvi proizvedeni čelik (površinski sloj željeza). Hlađenjem ovako obrađenog željeza (u pravilu pomoću neke tekućine) dobiveni materijal dobivao je elastičnost i čvrstoću, koja je bila nadmoćna osobinama nad broncom.
Željezo se počelo dobivati iz ruda, najvjerojatnije hematita (Fe2O3), oko 1500. pr. Kr., najprije u Anatoliji, današnjoj Maloj Aziji, kao tzv. spužvasto željezo. U to vrijeme, zbog nedovoljne temperature primitivnih peći, nije bilo moguće dobivanje lijevanog željeza, već je nastajalo spužvasto željezo, koje se kovanjem pretvaralo u upotrebljiv metal. Nalazišta u Uru (Irak), te u Egiptu svjedoče o ranom dobivanju željeza iz ruda. Željezo je u to vrijeme bilo nevjerojatno važan strateški materijal. Smatra se, da je pleme Hetita iz Male Azije postiglo svoju veliku vojnu moć upravo zbog rane proizvodnje željeznog oružja. U to je vrijeme cijena željeza bila veća od cijene zlata, a način njegovog dobivanja čuvao se kao najstroža tajna.
U staroj Grčkoj željezno doba počinje oko 1300. pr. Kr., a 1200. pr. Kr. željezo je već poznato u čitavom starom svijetu. Očvršćavanje željeza zakaljivanjem bilo je poznato oko 900. pr. Kr, a također i oporavljanje (popuštanje) zagrijavanjem. O tome svjedoče nalazi i pisani dokumenti iz Rima, Halstatta (Njemačka) i La Tene (Francuska).
Željezo je čovjeku bilo poznato već u prapovijesnim vremenima, a danas je ono kudikamo najvažniji tehnički metal. Od njega se prave mostovi, željeznice, strojevi, brodovi, građevine, itd. kao i bezbroj sitnica potrebnih u svakodnevnom životu: igle, čavli, vijci, pera, kvačice za spise, kutije za konzerve itd.
Dobivanje željeza
Za dobivanje željeza danas se uglavnom koriste oksidne, a rjeđe karbonatne rude. Crvena željezna ruda sadrži mineral hematit. Druge rude sadrže mineral magnetit, koji je crne boje i magnetičan. Željezo rijetko nalazimo u elementarnom obliku koji se nalazi u okolici vulkana i u meteorima. Velike količine željeza korištene od željeznog doba, u prvom tisućljeću prije Krista, dobivene su taljenjem željeznih minerala, kao što je hematit.
Iz oksidnih ruda željezo se dobiva redukcijom ruda koksom, odnosno ugljikovim(II) oksidom (ugljikov monoksid) u visokim pećima. Iz ruda koje su siromašne željezom (na primjer limonita), željezo se dobiva takozvanim kiselim taljenjem i Kruppovim postupkom.
Dobivanje željeza u visokim pećima
Kroz gornji otvor visoke peći (grotlo), peć se naizmjenično puni slojevima koksa i rude s talioničkim dodacima. Ovisno o rudi, talionički dodatak je vapnenac ili dolomit (ako su rude kisele, jer jalovine sadrže silikate i aluminijev oksid) ili kvarcni pijesak (ako su rude alkaline, jer jalovine sadrže kalcijev oksid). Najdonji sloj koksa se zapali, a dovodi mu se vruć zrak (do 800 °C) obogaćen kisikom. Pri tom koks izgara dajući najprije CO2, a zatim prolaskom kroz sljedeći sloj koksa prelazi u CO:
- 2 C + O2 → 2 CO
Nastali ugljikov(II) oksid (ugljikov monoksid) glavno je redukcijsko sredstvo koje postupno, ovisno o temperaturi pojedinih zona peći, sve više reducira okside željeza, dok konačno ne nastane tzv. spužvasto željezo, a sve reakcije se sumarno mogu svesti na:
- Fe2O3 + 3 CO → 2 Fe + 3 CO2
Reakcijama oslobođeni CO2 (koji nastaje raspadom karbonata) reagira s ugrijanim koksom dajući ponovo CO, koji se u manje vrućim dijelovima peći raspada na CO2 i fino dispergirani ugljik, koji se otapa u spužvastom željezu. Ugljik tako snizuje talište reduciranog željeza na 1100 - 1200 °C. Rastaljeno željezo se, zbog veće gustoće, slijeva polagano u donji dio peći i skuplja se na dnu odakle se ispušta u kalupe ili vagonete kojima se odvozi na daljnju preradu. Tekuća i lakša troska pliva na rastaljenom željezu i ispušta se kroz nešto više smješten ispust.
Proizvodi koji nastaju u visokoj peći su:
- Sirovo željezo. Polaganim hlađenjem dobiva se sivo sirovo željezo iz kojeg se izlučio grafit. Naglim hlađenjem dobiva se bijelo sirovo željezo iz kojeg se grafit nije stigao izlučiti. Međutim, sirovo željezo obično se ne hladi nego odmah prerađuje u čelike.
- Troska ili zgura, koja je uglavnom kalcijev alumosilikat, upotrebljava se za proizvodnju cementa i kao izolacijski materijal.
- Grotleni plin nastaje kao proizvod navedenih procesa gorenja, a sastoji se od dušika, ugljikovog dioksida, ugljikovog monoksida, vodika i metana. Koristi se za zagrijavanje zraka koji se upuhuje u peć.
Sirovo željezo
Sirovo željezo je zbog većeg sadržaja nečistoća i ugljika, jako krhko i nepodesno za obradu ili primjenu. Može se koristiti samo za lijevanje najgrubljih masivnih predmeta (npr. postolja), koji nisu mehanički ili toplinski opterećeni. Da bi se dobilo kvalitetnije željezo ili čelik, sirovo se željezo prerađuje, što uključuje smanjenje sadržaja svih primjesa i podešavanje željenog sadržaja ugljika, koji bitno određuje kvalitetu čelika. Čelikom se smatra legura željeza od 0,05 do 2,06% ugljika. Pročišćeno sirovo željezo koje sadrži više od 1,7%, a manje od 2,5% ugljika obično zovemo lijevano željezo, a koristi se za izradu masivnijih željeznih odljevaka za razna postolja, nosače, kostrukcijsko i građevinsko željezo itd. Mješanjem sirovog željeza s talinom kvarcnog pijeska i pretaljivanjem te smjese u pećima obloženim Fe2O3, u talini se dobiva spužvasto, porozno željezo, u kojem prisutni Fe2O3 oksidira većinu primjesa. Dobiva se tzv. profilno željezo jer se direktno iz peći, pod tlakom koji istiskuje silikatnu masu s otopljenim primjesama, izvlače profilni proizvodi željeza (cijevi, tračnice, šipke itd.).
Primjese znatno utječu na fizikalna svojstva željeza. Talište čistog željeza je 1535 °C, a željeza sa svega 0,83% ugljika 740 °C. Sastav sirovog željeza:
w(Fe) = 90%,
w(C) = 2 - 5%,
w(Si) = 0,2 – 4%,
w(P) = 0,1 – 3%,
w(Mn) = 1,5 – 6%,
w(S) = 0,01 – 0,05%.
Proizvodnja čelika
Postoji više postupaka prerade željeza u čelike, a najčešći su:[6]
- neposrednim propuhivanjem kisika ili zraka obogaćenog kisikom kroz rastaljeno željezo u konverterima. Najviše se koriste Bessemerov i Thomasov postupak. Razlikuju se u tome što se Thomasovim postupkom iz sirova željeza može ukloniti i fosfor.
- posrednom oksidacijom koja se provodi u Siemens - Martinovim pećima. Kod ovog postupka oksidaciju vrši kisik iz plinova iznad taline.
- LD postupkom s čistim kisikom (99,9%), u kojem se kisik ne provodi kroz talinu, nego provodi kroz vodom hlađenu kapljastu cijev, koja seže do jednog metra iznad taline. Danas se ovaj postupak sve više primjenjuje.
- elektrolučni postupak u kojem se sirovo željezo tali električnim lukom. Ovo je moderniji postupak dobivanja legiranih čelika u kojima je udio drugih metala veći od 5%.
Nalazišta
Željeza ima u sastavu Mjeseca, Sunca i drugih nebeskih tijela kao i na Zemlji gdje je najrasprostranjeniji metal. Zemljina se jezgra najvećim dijelom sastoji od kovinasta željeza, s nešto nikla, a upravo taj sastav željeza u vanjskoj tekućini jezgre i u njezinim čvrstim unutrašnjim dijelovima daje Zemlji njezino magnetno polje. Može se naći kao i mineral, ali rijetko, jer željezo se spremno spaja s kisikom i vodom pa stvara okside i druge minerale. Povremeno se nalazi u nekim promijenjenim bazaltima, gdje su željezni minerali svedeni na urođeno željezo.
Željezni cvijet ili željezni šešir nazivaju rudari dijelove ležišta željezne rude (pirita, hematita, magnetita, siderita), gdje su one prešle u limonite.
U prirodi (na mnogim mjestima Zemljine površine) spojeno se željezo nakupilo u većim koncentracijama, a stijene koje sadržavaju 20% i više željeza mogu služiti kao željezne rude. Najčešće i najvažnije rude od njih sadržavaju minerale hematit (Fe2O3 x H2O), najmanje zastupljen limonit (FeO(OH) x nH2O) i magnetit (Fe3O4) koje su oksidne rude, te vrlo rašireni pirit (FeS2) koji je sulfidna ruda, te siderit (FeCO3) koja je karbonatna ruda. Vivijanit je kristal, željezni fosfat. Željezo još nalazimo i u silikatnim rudama (spojevima).
Sve rude se moraju pržiti prije preradbe u sirovo željezo da prijeđu u oksid. Iz rude se sirovo željezo dobiva preradbom u visokoj peći. Tako dobiveno sirovo željezo upotrebljava se manjim dijelom za proizvodnju predmeta lijevanjem, a većim dijelom prerađuje se u čelik.
Zanimljivosti
- Za dobivanje 1 tone sirovog željeza potrebno je: 1,65 t rude s dodatcima, 0,5 t koksa, 1,5 – 2,5 t vrućeg zraka i 10 m3 vode za hlađenje. Pritom još nastaje: 0,3 t troske, 3 - 3,5 t grotlenih plinova i prašine.
- Eiffelov toranj sagrađen je 1889. Povodom svjetske izložbe u Parizu. Iako je Aleksandar Gustav Eiffel (1832.-1923.) imao najviše usjeha u projektiranju čeličnih mostova, njegov najznačajniji projekt je poznati pariški čelični toranj koji je po njemu dobio ime. Sa četiri rešetkasta nosača uzdiže se do visine oko 300 metara, a teži 9 700 tona. Čelični nosači spajaju tri platforme na visinama 58, 116 i 276 metara koje su posjetiteljima pristupačne dizalom ili stubama. S jedne od turistički najpoznatijih građevina na svijetu pruža se pogled oko 140 km u daljinu. Na tornju se nalazi meteorološka postaja, a služi i kao antenski stup.
Izvori
- Hrvatska enciklopedija, Broj 11 (Tr-Ž), str. 400.. Za izdavača: Leksikografski zavod Miroslav Krleža, Zagreb 2000.g. ISBN 953-6036-32-0 .
- ↑ željezo, [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2019.
- ↑ [2] "Fizikalna metalurgija I", dr.sc. Tanja Matković, dr.sc. Prosper Matković, www.simet.unizg.hr, 2011.
- ↑ [3] "Elementi u tragovima - željezo", Iz knjige: prof. dr. Roko Živković "Dijetoterapija", www.zzjzpgz.hr, 2011.
- ↑ [4] "ŽELJEZO, Fe", www.pse.pbf.hr, 2011.
- ↑ Hrvatska enciklopedija (LZMK); broj 11 (Tr-Ž), str. 478. Za izdavača: Leksikografski zavod Miroslav Krleža, Zagreb 2009.g. ISBN 978-953-6036-41-7
- ↑ "Strojarski priručnik", Bojan Kraut, Tehnička knjiga Zagreb 2009.
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | As | Br | Kr | ||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Te | I | Xe | |||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Rn | ||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| Alkalijski metali | Zemnoalkalijski metali | Lantanoidi | Aktinoidi | Prijelazni metali | Slabi metali | Polumetali | Nemetali | Halogeni elementi | Plemeniti plinovi |


