Benzen
| Benzen C6H6 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC nomenklatura | benzen | ||||||||||
| Ostala imena | cikloheksa-1,3,5-trien, stariji naziv benzol | ||||||||||
| Identifikacijski brojevi | |||||||||||
| Osnovna svojstva | |||||||||||
| Molarna masa | 78.11 g·mol−1 | ||||||||||
| Relativna molekulska masa | 78.11 | ||||||||||
| Izgled | prozirna, bezbojna tekućina specifičnog mirisa | ||||||||||
| Gustoća |
0.8765(20) g·cm−3 | ||||||||||
| Talište | 278.7 K 5.5 °C | ||||||||||
| Vrelište | 353.3 K 80.1 °C | ||||||||||
| Tlak para |
75 mmHg @20ºC | ||||||||||
| Topljivost u vodi |
1.8 g·l−1 (15 °C), H2O | ||||||||||
| Dipolni moment |
0 D | ||||||||||
| Struktura | |||||||||||
| Oblik molekule | šesterokut | ||||||||||
| Sigurnosne upute | |||||||||||
| |||||||||||
| SI-sustav mjernih jedinica korišten je gdje god je to moguće. Ukoliko nije drugačije naznačeno, upisane vrijednosti izmjerene su pri standardnim uvjetima. | |||||||||||
Benzen (prema njem. Benzoe: benzojeva smola < arap. luban gawi: javanski tamjan) je najjednostavniji aromatski ugljikovodik. Molekulska formula mu je C6H6.
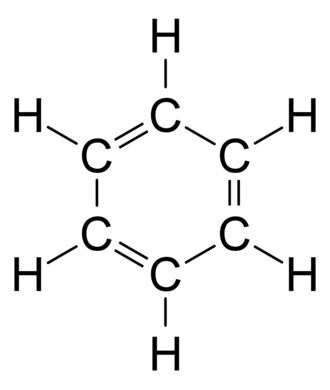
Osobine i svojstva
Iz brojevnog omjera atoma ugljika i vodika može se zaključiti da je benzen nezasićeni ugljikovodik, ali se pokazalo da se po kemijskim svojstvima od njih znatno razlikuje. Znanstvenici su dugo pokušavali odrediti strukturnu formulu. Njemački kemičar Friedrich August Kekulé von Stradonitz predložio je 1865. godine šesterokut s naizmjence postavljenim jednostrukim i dvostrukim kovalentnim vezama između atoma ugljika, a danas se upotrebljava njegova ili Thieleova formula, ovisno o potrebi.
Može se smatrati rezonantnim hidridom Kekuleovih i Dewarovih struktura.
Po nekim je svojstvima sličan zasićenim ugljikovodicima (postojan prema oksidima; burno reagira sa sumpornom i dušičnom kiselinom).
Benzen je pri sobnoj temperaturi bezbojna, lako hlapljiva, zapaljiva i otrovna tekućina, jakog karakterističnog mirisa.
Vrije pri 80.1 °C, dok pri temperaturi nižoj od 5.5 °C prelazi u čvrsto stanje (tj. skrućuje se u bijelu kristalnu tvar).
U vodi je praktički netopljiv, ali se vrlo dobro otapa u mnogim organskim otapalima (benzinu, alkoholu, eteru, itd.). I sam je dobro organsko otapalo, otapa masti i ulja, smole i boje.
Zapaljen, na zraku gori svijetlim i vrlo čađavim plamenom, a uz dovoljan pristup kisika potpuno izgara u ugljikov(IV) oksid i vodu:
- 2C6H6 + 15O2 → 12CO2 + 6H2O
Opasnosti:
- Benzen je otrovan, a osobito njegove pare, a kronično izlaganje kod životinja uzrokuje kancerogena oboljenja, najčešće leukemiju.
- Lako je zapaljiv, a pomiješan sa zrakom stvara eksplozivnu smjesu.
- U pićima s benzojevom i askorbinskom kiselinom nastaje jako malo i neprimjetno benzena.
Derivati benzena (proizvodi dobiveni iz benzena) nisu otrovni kao benzen, pa se u industriji rabe kao njegova zamjena.
Benzenov prsten
Benzenski prsten prema Kekuleovoj formuli, sastavljen je od 6 atoma ugljika koji su vezani međusobno, naizmjence jednostrukim i dvostrukim vezama, a također i sa 6 atoma vodika.
Benzenski prsten sastavni je dio svih benzenoidnih aromatskih spojeva; u strukturnim formulama obično se skraćeno prikazuje kao pravilan šesterokut s upisanom kružnicom (tzv. benzenov prsten). Također može se crtati i s jednostrukom vezom između atoma ugljika.
Svi aromatski ugljikovodici imaju jedan ili više benzenovih prstenova.
Supstitucija
Podliježe supstitucijskim reakcijama u kojima se vodikovi atomi zamjenjuju drugim atomima ili skupinama. Tako ponašanje posljedica je delokalizacije p-elektrona unutar benzenskoga prstena, te su sve veze između ugljikovih atoma u benzenu ekvivalentne, po duljini između jednostruke i dvostruke veze.
Halogeniranje: Halogeni element (X - Cl,Br) reagira s benzenom, pri čemu nastaju odgovarajući derivat benzena i odgovarajući halogenovodik (HX):
- C6H6 + X2 → C6H5X + HX

Nitriranje: Smjesa koncentrirane dušične i sumporne kiseline reagira s benzenom pri čemu nastaju nitrobenzen i voda:
- C6H6 + HNO2 (uz oleum kao katalizator) → C6H5NO2 + H2O
Sulfoniranje: Otopina sumporovog(VI) oksida u sumpornoj kiselini, poznata kao oleum ili dimeća sumporna kiselina reagira s benzenom pri čemu nastaje benzensulfonska kiselina. Njezine soli se nazivaju benzensulfonati.
- C6H6 + SO3 (uz conc. H2SO4 kao katalizator) → C6H5SO3H
Alkiliranje: Reakcijom halogenalkana (R-X) s benzenom uz odgovarajući bezvodni aluminijev halogenid (AlX3) kao katalizator, nastaju alkalirani benzen i halogenovodik:
- C6H6 + CH3CH2X (uz AlX3 kao katalizator) → C6H5CH2CH3 + HX
Adicija
Sadržava nezasićene veze, ali ne podliježe lako reakcijama adicije.
Benzen se pri visokoj temperaturi i tlaku može katalitički hidrogenirati uz nikal kao katalizator, pri čemu nastaje cikloheksan.
- C6H6 + 3H2 (150°C i Nikl kao katalizator) → C6H12
Prilikom kloriranja benzena, potrebno je ultraljubičastim zračenjem dobiti radikale klora. Produkt reakcije je 1,2,3,4,5,6-heksaklorcikloheksan, poznat i kao lindan.
- C6H6 + 3Cl2 (hv)→ C6H6Cl6
Dobivanje
Prvi ga je izdvojio Michael Faraday 1825. godine suhom destilacijom kamenog ugljena.
- Frakcijskom destilacijom katrana kamenog ugljena
- Sintetski; Sintezom tri molekule etina (acetilena, C2H2):
- 3 HC≡CH → C6H6
- Dekarboksilacijom benzojeve kiseline
Uporaba

Upotrebljava se u kemijskoj industriji kao važno otapalo (otapa masti i ulja, smole, boje, itd.), kao polazna sirovina za dobivanje mnogih aromatskih spojeva. Od benzena se izvodi i velika skupina organskih spojeva (benzenoidni aromatski spojevi). Služi za proizvodnju lijekova, boja, lakova, plastičnih masa, eksploziva, sredstava za pranje, pesticida.
Benzen se sve više izbjegava u industriji jer je otrovan i kancerogen je. Upravo zbog njegovog štetnog djelovanja u nekim ga industrijskim procesima, zamjenjuju ga njegovi derivati koji nisu toliko štetni za ljudsko zdravlje (npr. toluen ili ksilen).
Derivati benzena
Spojevi koji sadrže benzenov prsten
Izvori
- Hrvatska enciklopedija, Broj 2 (Be-Da), str. 57.. Za izdavača: Leksikografski zavod Miroslav Krleža, Zagreb 2000.g. ISBN 953-6036-32-0