Hlapljenje
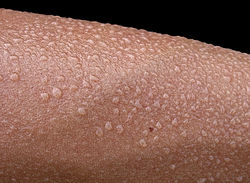


Hlapljenje je prelaženje kemijske tvari iz tekućega u plinovito agregatno stanje bez vrenja, na temperaturi nižoj od vrelišta. Iako na temperaturi nižoj od vrelišta prosječna kinetička energija molekula tekućine nije dovoljna za napuštanje tekućine, neke, najbrže, molekule imaju dovoljnu kinetičku energiju da se mogu odvojiti od površine tekućine i nastaviti se gibati slobodno. Hlapljenjem se prosječna kinetička energija molekula u tekućini smanjuje i temperatura tekućine opada. Brzina hlapljenja veća je što je viša temperatura tekućine i niži tlak izvan tekućine. [1] Hlapljenje je to veće što je veća površina tekućine, što je veća brzina vjetra iznad tekućine (propuh) i što je viša temperatura. Osim toga, hlapljenje ovisi o vrsti tekućine, na primjer alkohol hlapi brže od vode, a eter još brže od alkohola. [2]
Iako na tim temperaturama prosječna kinetička energija molekula tekućine nije dovoljna za promjenu agregatnog stanja, neke (najbrže) molekule imaju dovoljnu energiju da se mogu odvojiti od površine i nastaviti se gibati u zraku. Tako tekućina postupno isparava i na temperaturama nižim od vrelišta (na primjer sušenje rublja). Hlapljenjem se prosječna kinetička energija molekula tekućine smanjuje i njezina temperatura opada (na primjer tako se hlapljenjem znoja ljudsko tijelo hladi). Također, slobodne molekule pare u zraku koje udare u površinu tekućine mogu izgubiti dovoljno energije da se vrate u tekućinu pa se uspostavlja dinamička ravnoteža (npr. kad je velika vlažnost zraka sušenje rublja i hlađenje ljudskoga tijela znojenjem je usporeno).
Isparavanje[uredi | uredi kôd]
Isparavanje je prijelaz tvari iz tekućeg u plinovito agregatno stanje. Prema kinetičko-molekularnoj teoriji topline, tekućina isparuje kada njezine molekule zagrijavanjem poprime dovoljno energije da nadvladaju kohezijske sile unutar tekućine i tlak nad njezinom površinom. Razlikuje se isparavanje vrenjem i hlapljenjem. Tekućina isparuje vrenjem kada se tlak pare u tekućini izjednači s ukupnim tlakom nad tekućinom. Temperatura pri kojoj tekućina vrije naziva se vrelištem. Povećavanjem tlaka nad tekućinom vrelište raste, a smanjenjem tlaka opada. Tekućina isparuje hlapljenjem kada je tlak pare u tekućini veći od parcijalnoga tlaka te pare nad tekućinom, a manji od ukupnoga tlaka nad tekućinom; tekućina, dakle, hlapi pri temperaturi nižoj od vrelišta.
Jedna je od najstarijih primjena isparavanja dobivanje soli iz morske vode. U procesnoj se tehnici pod isparavanjem razumije tehnološka operacija kojom se u isparivaču dio otapala vrenjem prevodi u plinovito (parovito) stanje kako bi se povećala koncentracija otopine (uparavanje), na primjer pri proizvodnji šećera, različitih soli, umjetnih gnojiva i drugog. Otopina se zagrijava u dijelu isparivača koji se naziva ogrjevnom komorom, a para otapala, koja se naziva supara, izlazi iz otopine u parni prostor isparivača. Danas se uglavnom rabe cijevni isparivači, u kojima otopina prirodno ili prisilno cirkulira kroz vruće cijevi i isparuje se uz vrenje ili se isparuje u tankom sloju na stijenkama cijevi. Isparivači se najčešće zagrijavaju svježom vodenom parom (jednostruko iskorištavanje topline uz stalan tlak) ili, ako su isparivači međusobno povezani u niz, suparom iz prethodnog isparivača. Tako se toplina višestruko iskorištava, jer se supara iz prvog isparivača upotrebljava za zagrijavanje drugog i tako dalje, ali je to moguće ako je u svakom idućem isparivaču tlak niži od prethodnoga, pa je i vrelište otopine sve niže, ili ako se termokompresijom stalno povećava temperatura supare. Utrošak topline za zagrijavanje otopine može se smanjiti i ako se sirovina predgrijava već zagrijanim produktom koji izlazi iz isparivača. Osim za opisano uparavanje, kojemu je cilj dobivanje otopine veće koncentracije, isparavanje se primjenjuje i radi dobivanja čistog otapala (na primjer pitke vode pri odsoljavanju vode ili desalinizaciji morske vode) te kao proces kojim se postiže učinak hlađenja u rashladnim strojevima. [3]
Izvori[uredi | uredi kôd]
- ↑ hlapljenje, [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2017.
- ↑ Velimir Kruz: "Tehnička fizika za tehničke škole", "Školska knjiga" Zagreb, 1969.
- ↑ isparavanje, [2] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2015.