Ugljikov (II) oksid
| Ugljikov (II) oksid | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
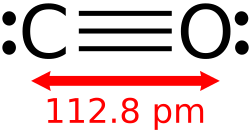 | |||||||||||
| IUPAC nomenklatura | Ugljikov monoksid | ||||||||||
| Ostala imena | Ugljični monooksid Ugljikov (II) oksid | ||||||||||
| Identifikacijski brojevi | |||||||||||
| Osnovna svojstva | |||||||||||
| Molarna masa | 28.010 g/mol | ||||||||||
| Izgled | bezbojni plin bez mirisa | ||||||||||
| Gustoća |
789 kg/m3, tekućina | ||||||||||
| Talište | 68,13 K -205,02 °C | ||||||||||
| Vrelište | 81,6 K -191,5 °C | ||||||||||
| Topljivost u vodi |
27,6 mg/L (25 °C) | ||||||||||
| Dipolni moment |
0.122 D | ||||||||||
| Struktura | |||||||||||
| Sigurnosne upute | |||||||||||
| |||||||||||
| SI-sustav mjernih jedinica korišten je gdje god je to moguće. Ukoliko nije drugačije naznačeno, upisane vrijednosti izmjerene su pri standardnim uvjetima. | |||||||||||
Ugljikov(II) oksid (ugljikov monoksid)[1] kemijski je spoj jednog atoma ugljika i jednog atoma kisika, formulom izraženo CO.
To je plin bez boje i mirisa koji nastaje nepotpunim izgaranjem tvari u kojima ima ugljika, te je jako otrovan jer se veže na hemoglobin u krvi čime spriječava prijenos kisika (često zvan "tihi ubojica").
Dobivanje
Ugljikov(II) oksid nastaje najčešće nepotpunom oksidacijom ugljika iz fosilnih goriva.
2 C(s) + O2(g) --> 2 CO(g)
U prirodi se pojavljuje kao sastojak vulkanskih plinova. To je vrlo otrovan plin, bez boje i mirisa, nešto lakši od zraka. Slabo je topljiv u vodi, ubrajamo ga u neutralne okside, a gori svijetloplavim plamenom.
Važna je industrijska sirovina. Pri povišenoj temperaturi i tlaku vrlo je reaktivan, lako se oksidira, pa se koristi kao reducens, posebno u metalurgiji za dobivanje metala iz oksidnih ruda. Pri dobivanju željeza, ali i pri drugim procesima redukcije, važna je reverzibilna reakcija disproporcioniranja ugljikova monoksida.
Ugljikov monoksid dobiva se najčešće u smjesi s drugim plinovima kao generatorski plin (gorivo oko 1100 kcal/m3, sadrži 30% CO i 60% N2) ili vodeni plin, koji nastaju provođenjem zraka ili vodene pare preko užarenog koksa.
2 C(s) + 4 N2(g) + O2Tekst indeksa(g) --> 2 CO(g) + 4 N2(g)
C(s) + H2O(g) --> CO(g) + H2(g)
Oba plina se često upotrebljavaju kao industrijsko gorivo zbog velike egzotermnosti izgaranja ugljikova(II) oksida.
2 CO(g) + O2(g) --> 2 CO2(g)
Ugljikov monoksid čuva se pod tlakom u posudama od bakra, aluminija ili nikla i njihovih slitina, tj. tvari s kojima ne tvori otrovne spojeve.
Ugljikov monoksid je krvni otrov, jer je afinitet ugljikova(II) oksida prema hemoglobinu 200-300 puta veći od afiniteta kisika.
Vezanje ugljikova(II) oksida za hemoglobinsko željezo onemogućava vezanje kisika i na taj način sprječava normalnu opskrbu stanica kisikom.
Znakovi trovanja su: glavobolja, vrtoglavica, lupanje srca, opća slabost, šum u ušima, a mogu se javiti: apatija, zbunjenost, nesvjestica i grčenje. Ako je volumni udio ugljikova(II) oksida u zraku 0,2 do 0,4%, dolazi do gubitka svijesti, a nakon duljeg vremena i do smrti. Prva pomoć pri trovanju ugljikovim(II) oksidom je iznošenje otrovanoga na svjež zrak, umjetno disanje i udisanje kisika.
Već je 100 ppm CO u zraku štetno po zdravlje.
Pušači imaju u krvi 2 do 5 puta veću koncentraciju ugljikova(II) oksida nego nepušači.
Sadržaj ugljikova(II) oksida, ali i drugih štetnih plinova u zraku određuje se pomoću posebnih indikatorskih cjevčica. Određeni volumen plina koji se ispituje provlači se kroz cjevčicu pomoću posebne pumpice. U cjevčicama je na površinu porozne mase nanesen specifičan reagens koji mijenja boju ako se u zraku nalazi ispitivani plin. Nakon 10 usisaja pumpicom na cjevčici se izravno odčita sadržaj tog plina u 1m3 zraka.
Izvori
- ↑ Vladimir Simeon, Hrvatska nomenklatura anorganske kemije, Školska knjiga, Zagreb, 1996., 59.
- Udžbenik za treći razred gimnazije „Anorganska kemija“, Sandra Habuš – Dubravka Stričević – Vera Tomašić. Izdavač: PROFIL INTERNATIONAL, tisak: tiskara Meić, Uporabu udžbenika odobrilo je Ministarstvo prosvjete i športa Republike Hrvatske rješenjem KLASA: *, od 3. srpnja 1998.g..



