Spektroskopija




Spektroskopija je znanstvena djelatnost koja se bavi spektrima kao odrazom energijskih ili strukturnih promjena u atomima i molekulama kemijskih tvari nakon njihova međudjelovanja s elektromagnetskim zračenjem ili sa subatomskim i drugim česticama. Najčešće se radi o razotkrivanju (detekciji), tumačenju i primjeni spektara koji su u vezi s elektromagnetskim zračenjem. Pritom se obično mjeri jakost (intenzitet) emitiranog (emisijski spektar), apsorbiranog (apsorpcijski spektar) ili raspršenoga zračenja (raspršenje) ovisno o njegovoj valnoj duljini, odnosno frekvenciji. U atomima i molekulama postoji više energijskih razina, a energija emitiranog ili apsorbiranoga zračenja odgovara razlici među tim razinama. Zračenje se emitira prelaskom s više na nižu energijsku razinu, a apsorbira se prelaskom s niže na višu razinu. Kako je skup energijskih razina svojstvo atoma i molekula određene kemijske tvari, razotkrivanjem i tumačenjem spektara zračenja mogu se dobiti podatci o kemijskom sastavu i strukturi tvari (spektrometrijska analiza), ali i spoznaje o uzbuđenom stanju, elektronskoj, vibracijskoj i rotacijskoj energiji, atomskim i molekularnim energijskim prijelazima, kemijskoj vezi i drugo. [1]
Među najvažnije spektroskopske tehnike koje se temelje na međudjelovanju tvari s elektromagnetskim zračenjem ubrajaju se:
- spektroskopija na apsorpciji i na emisiji zračenja:
- spektroskopija ultraljubičastoga zračenja (UV) i vidljivoga zračenja,
- spektroskopija infracrvenoga zračenja (IR),
- spektroskopija rendgenskoga zračenja (rendgenska spektroskopija) i gama-zračenja (Mössbauerov učinak);
- spektroskopija samo na apsorpciji:
- spektroskopija mikrovalnoga zračenja,
- spektroskopija elektronske paramagnetske rezonancije (EPR ili ESR),
- spektroskopija nuklearne magnetske rezonancije (NMR) te
- fotoelektronska spektroskopija;
- spektroskopija samo na emisiji:
- spektroskopija fluorescencije;
- na raspršenju:
- na polarizaciji:
- spektroskopija optičke rotacijske disperzije (ORD) i
- cirkularnoga dikroizma (CD).
Najvažnije spektroskopske tehnike koje se temelje na međudjelovanju tvari sa subatomskim i drugim česticama (elektroni, protoni, neutroni, ioni) jesu:
Uvođenjem lasera kao izvora zračenja mnogostruko se povećala osjetljivost mnogih spektroskopskih tehnika i moć razlučivanja spektara (laserska spektroskopija) te su proširene mogućnosti istraživanja strukture atoma i molekula.
Spektroskopija se primjenjuje u mnogim granama prirodnih znanosti jer daje podatke o građi i sastavu tvari, njezinoj temperaturi, tlaku. Spektroskopija može dati informacije o dinamici promatranog sustava. Vjerojatno najšira upotreba spektroskopije je u analitičke svrhe. Spektroskopija se najčešće dijeli prema spektralnom području, a to često ovisi o grani znanosti koja rabi dotičnu spektroskopiju. Kao rezultat spektroskopskog istraživanja dobiva se spektar. Spektroskopija se, prema pojavi koji izaziva sprezanje elektromagnetskog zračenja može podijeliti na:
Međudjelovanje elektromagnetskog zračenja i materije
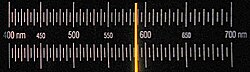
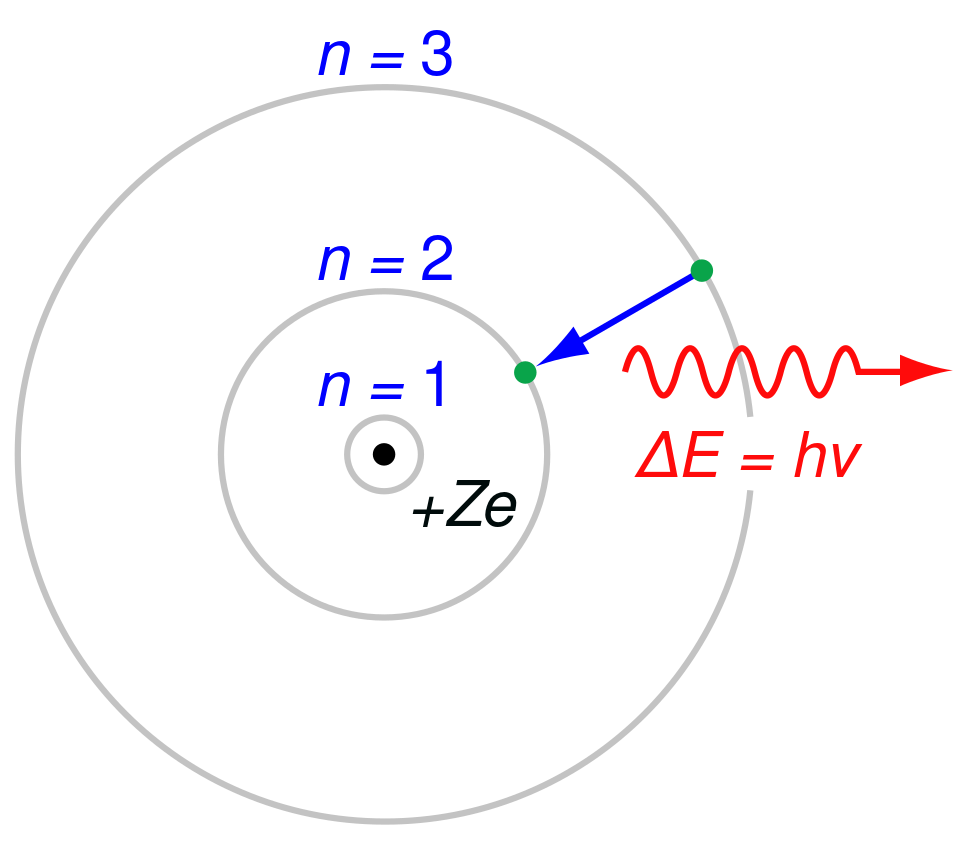
Sve pojave koje se promatraju u spektroskopiji, objašnjavaju se s nekoliko mogućih pojava međudjelovanja elektromagnetskog zračenja i materije. Sustav koji stupa u međudjelovanje s elektromagnetskim zračenjem mora sadržavati diskretne energijske razine. Po Bohrovom uvjetu, razlika između energijskih razina sustava mora biti jednaka energiji fotona elektromagnetskog zračenja koji stupa u međudjelovanje sa sustavom. Ovisno o tipu međudjelovanja (interakcije) razlikuju se 3 pojavna oblika spektra: kontinuum, linija i vrpca. Sunce i zagrijane krutine emitiraju šire područje elektromagnetskoga zračenja svih valnih duljina ili frekvencija, dajući kontinuirani spektar. Naprotiv, pobuđeni atomi u plinovitoj fazi emitiraju zračenje samo međusobno strogo odvojenih pojedinačnih frekvencija, što daje linijski spektar. Svaki kemijski element emitira svojstvene linije koje ga razlikuju od ostalih elemenata, pa se linijski spektri nazivaju atomskim spektrima. Treći je oblik vrpčasti spektar (spektroskopska vrpca), koji nastaje tako što se dio zračenja pri prolasku kroz uzorak apsorbira samo pri nekim valnim duljinama. Takvi apsorpcijski spektri sastoje se od vrpci koje odgovaraju specifičnoj apsorpciji u uzorku; to su pretežno molekularni spektri koji se zapažaju u širem dijelu elektromagnetskoga spektra. Apsorpcijom ultraljubičastog i vidljivoga dijela elektromagnetskoga zračenja nastaju apsorpcijski elektronski spektri, infracrvenoga zračenja vibracijski, mikrovalnoga rotacijski, radiovalnoga spektri elektronske paramagnetske rezonancije i nuklearne magnetske rezonancije i tako dalje. Na navedenim razlikama temelji se i podjela spektroskopije na pojedine instrumentalne tehnike.

Apsorpcija zračenja
Sustav apsorbira foton. Poslije apsorpcije zračenja, sustav ostaje u pobuđenom stanju.

Spontana emisija
Sustav, koji je u pobuđenom stanju, spontano se vraća u osnovno stanje ili pobuđeno stanje niže energije, emitiranjem fotona. Energija fotona, po Bohrovom uvjetu, odgovara razlici energija stanja sustava prije i poslije spontane emisije.

Stimulirana emisija
Sustav u pobuđenom stanju, intereagira s fotonom, čija je energija jednaka energiji pobuđenog stanja, emitiranjem novog fotona. Emitirani foton je koherentan s fotonom koji je izazvao interakciju: fotoni imaju jednaku energiju, fazu, smjer i usmjerenje.

Rayleighovo raspršenje
Foton koji odlazi od sustava, nakon Rayleighovog raspršenja, ima istu energiju kao i foton koji je došao na sustav, ali ima različit smjer. Sustav ima jednaku energiju prije i poslije Rayleighovog raspršenja.

Ramanovo raspršenje
Foton koji odlazi od sustava nema jednaku energiju kao i foton koji je došao na sustav. Sustav Ramanovim raspršenjem dobiva ili gubi energiju. Razlika u energiji sustava, prije i nakon Ramanovog raspršenja odgovara razlici energija dolazećeg i odlazećeg fotona. Ako odlazeći foton ima nižu energiju od dolazećeg fotona (sustav je raspršenjem dobio energiju), raspršenje se naziva Stokesovo raspršenje, u suprotnom slučaju raspršenje se naziva antistokesovo raspršenje.
Ionizacija
Foton se apsorbira na sustavu (atomu, molekuli, kristalu ...), a njegova energija se troši na emitiranje elektrona. Sustav se nakon ionizacije obično nalazi u pobuđenom stanju. Energija fotona je jednaka sumi energija vezanja elektrona za sustav, kinetičke energije elektrona i razlici energija sustava prije i posije ionizacije. Ionizacija se može dogoditi jedino ako je energija fotona veća od energije vezanja elektrona za sustav.

Augerov efekt
Foton se apsorbira na sustav pobuđivanjem sržnog elektrona u neko pobuđeno stanje. Sustav se relaksira emisijom drugog elektrona koji ima manju energiju vezanja (valentnog elektrona). Augerov efekt se razlikuje od ionizacije jer emitirani elektroni imaju točno određene kinetičke energije.
Comptonov efekt
Foton se neelastično sudari s elektronom (ili nekom drugom česticom), pri čemu se dio energije fotona prenese na elektron. Suma energije fotona i kinetičke energije elektrona prije sudara mora biti jednaka istoj sumi poslije sudara. Pri kvantnoj teoriji pri sudaru jedan dio energije elektronu slično kao pri elastičnom sudaru klasičnih čestica pa je njegova energija nakon rasijanja E*<E prije rasijanja.
Stvaranje parova
Interakcijom fotona s materijom stvaraju se parovi čestica-antičestica. Energija fotona troši se na masu para čestica-antičestica i na njihovu kinetičku energiju. Prema tome stvaranje parova se može dogoditi samo onda kada je energija fotona veća od energije koja je ekvivalentna masi para čestica-antičestica.
Opći principi
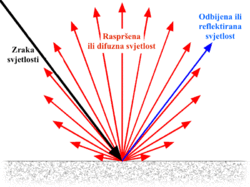
Za svako snimanje spektra, potrebno je imati: Izvor zračenja, uzorak, monokromator i detektor. Elektromagnetsko zračenje se iz izvora usmjerava na uzorak, koji može apsorbirati, raspršiti, ili reflektirati svjetlo. Ako uzorak emitira zračenje, izvor zračenja je sam uzorak. Zračenje sa uzorka se vodi prema monokromatoru, koji propušta samo jednu valnu duljinu prema detektoru. Detektor primljeno zračenje pretvara u signal, koji se može zapisati kao spektar. Kao monokromator se u novije vrijeme upotrebljava Michaelsonov interferometar koji propušta više valnih duljina u danom vremenu. Spektar koji se dobije pomoću Michaelsonovog interferometra se naziva spektar u vremenskoj domeni, a primjenom matematičkog postupka Fourierove transformacije taj se spektar pretvara u spektar u frekvencijskoj domeni, koji je jednak spektru dobivenim klasičnim monokromatorom.
Spektroskopija vidljivog zračenja
Spektroskopija vidljivog zračenja upotrebljava vidljivu svjetlost kao medij proučavanja.
Vidljivo zračenje uzrokuje pobuđenje elektona unutar atoma, molekula, kristalnih tvari ili amorfnih tvati. Spektroskopijom vidljivog zračenja se proučavaju efekti prouzrokovani promjenom elektronske strukture atoma ili molekula te njihova elektronska struktura, kao i elektronska struktura kristaliničnih i amorfnih tvari. Vidljivo zračenje emitiraju objekti čija je toplinska energija atoma ili molekula jednaka ili veća energiji pobuđenja njihovih elektrona. Ti objekti moraju biti na temperaturi većoj od oko 1000 ºC.
U kemiji ova spektroskopija obuhvaća i blisko ultraljubičasto zračenje, jer se za to optičko područje upotrebljavaju iste tehnike i isti materijali, a instrumenti često mogu snimati spektre u oba spektralna područja. Takva spektroskopija se označava kraticom UV-VIS (eng. UltraViolet-VISible).
Dio astronomije koji proučava vidljivo zračenje se naziva optička astronomija.
Izvori zračenja
Kao izvori zračenja služe volframove žarulje, halogene žarulje, ksenonske žarulje. U ultraljubičastom području rabe se deuterijske lampe. Kao izvor zračenja može poslužiti i laser čija se valna duljina može ugađati. U slučaju lasera, nije potreban monokromator, jer laser emitira zračenje točno određene valne duljine, koja je puno bolja od svjetlosti koja izlazi iz monokromatora. Spektroskopija koja se služi laserom naziva se spektroskopija visokog razlučivanja. Sinkrotronsko zračenje iz sinkrotrona primjenjuje se kao izvor zračenja jer pokriva široko spektralno područje, i velikog je intenziteta. Ponekad se može rabiti svjetlo plamena ili iskre.
Optički elementi
U optičkoj astronomiji najčešće se upotrebljavaju aluminizirana ili posrebrena zrcala. U kemiji, gdje se ujedno proučava i blisko ultraljubičasto zračenje, najčešće se primjenjuje kvarcno staklo, koje propušta i vidljivo i blisko ultraljubičasto zračenje. U specijalnim slučajevima primjenjuju se i drugi materijali, npr. safir. Uzorak se stavlja u specijalne posudice: kivete. Ako uzorak slabo apsorbira zračenje upotrebljavaju se kivete sa sustavom aluminijskih, srebrnih ili zlatnih zrcala koje mogu povećati optički put svjetla i na više desetaka metara. Uzorci se često analiziraju kao vodene otopine.
Monokromator
Kao monokromator se najčešće upotrebljava optička rešetka. U starijim se instrumentima rabila i optička prizma, ali ona je nepraktična jer ima nelinearan lom svjetla.
Detektor
Prvi detektor koji se upotrebljavao bilo je oko. Prvi spektroskopski uređaji bili su jednostavni monokromatori pred koje se stavljao osvijetljeni uzorak. Takav uređaj se naziva spektroskop (grčki skopeo = gledam). Fotografski film i fotografske ploče rabe se u spektroskopskim uređajima nazvanim spektrografi (grčki grafo = pišem). U modernim spektroskopskim uređajima, spektrometrima i spektrofotometrima, upotrebljavaju se fotomultiplikatori, a rjeđe fotoosjetljive diode i CCD detektori.
Spektroskopija infracrvenog zračenja
Spektroskopija infracrvenog zračenja (IR spektroskopija) primjenjuje infracrveno zračenje kao medij proučavanja.
Infracrveno zračenje emitiraju molekule zahvaljujući svojim vibracijama. Apsorbiranjem infracrvenog zračenja molekulske vibracije se pobuđuju, pa molekule počinju jače vibrirati. Zbog toga se infracrvena spektroskopija, zajedno s ramanovom spektroskopijom zove vibracijska spektroskopija. Slobodni atomi ne emitiraju infracrveno zračenje. Svaka molekula ima karakteristične vibracije, koje ovise o čvrstoćama veza i masama dijelova molekula koje vibriraju. Ta činjenica daje infracrvenoj spektroskopiji velike analitičke mogućnosti jer je moguće odrediti od kojih se funkcionalnih skupina molekula sastoji. Kako svaka molekula ima različiti infracrveni spektar, infracrvena spektroskopija se primjenjuje pri identifikaciji tvari. Kako je toplinska energija molekula veća od energije vibracija, infracrveno zračenje emitiraju objekti zahvaljujći svojoj toplinskoj energiji. Valna duljina emitiranog zračenja ovisi o temperaturi prema zakonu crnog tijela.
Izvori zračenja
Kao izvor zračenja upotrebljavaju se Nernstov ili Globarov štapić. to su komadi keramike koji se zagrijavaju na određenu temperaturu.
Optički elementi
Optički elementi se obično rade od kristala natrijevog klorida, kalijevog klorida i sličnih soli, a najčešće kalijevog bromida. litijev fluorid je proziran u najvećem dijelu spektra. Ovi materijali lako reagiraju s vlagom iz zraka, pa brzo postaju zamućeni, pa ih je potrebno polirati prije upotrebe. Tekući uzorci rabe se između dviju pločica kalijevog bromida ili neke druge soli, u obliku tankog filma. Kruti uzorci se samelju u prah i pomiješaju s prahom kalijevog bromida. Dobivena smjesa se spreša u pastilu, koja se stavlja u spektrofotometar. Prah krutih uzoraka može se pomiješati i s organskom tekućinom i upotrebljavati kao i tekući uzorak, ali tada se, prilikom analize spektara, treba paziti na dijelove spektra koje je uzrokovala organska tekućina. Vodene otopine se nikad ne rabe jer voda apsorbira infracrveno zračenje, a materijali od kojih su napravljeni optički elementi su jako topljivi u vodi.
Monokromator
Monokromator je najčešće optička rešetka, kao i kod spektroskopije vidljivog zračenja. Prizme se rijetko upotrebljavaju jer moraju biti napravljene od kristala neke soli.
Detektor
Detektor je termoosjetljivi otpornik, termistor. U specijalnim slučajevima se primjenjuje bolometar: metalni balon ispunjen plinom. Promjena temperature, uzrokovana infracrvenim zračenjem se detektira promjenom volumena plina u balonu.
Ramanova spektroskopija


Ramanova spektroskopija primjenjuje neelastično raspršenje svjetlosti, Ramanovo raspršenje za prikupljanje spektroskopskih podataka. Elektromagnetsko zračenje, raspršeno na molekuli, sadrži dvije komponente koje dolaze od vibracija ili rotacija molekula. Ramanovi spektrofotometri koriste izvor monokromatskog zračenja koje je usmjereno na uzorak. Zračenje, raspršeno pod nekim kutem (obično pod 90º) vodi se na monokromator, iz kojeg se propušta samo jedna valna duljina. Skeniranjem u području valnih duljina oko valne duljine izvora zračenja, dobiva se spektar. Spektar se sastoji od jedne linije velike jakosti, koja odgovara valnoj duljini upadnog zračenja (Rayleighovo raspršenje), te skupa vrpci i/ili linija pri većim valnim duljinama (antistokesovo raspršenje) i skupine vrpci i/ili linija pri manjim valnim duljinama (Stokesovo raspršenje) puno manje jakosti. Te skupine linija odgovaraju vibracijskom i/ili rotacijskom spektru molekule. Energija spektroskopskog prijelaza se određuje razlikom energija iz Stokesove ili antistokesove vrpce i valne duljine upadnog, monokromatskog zračenja. Kako su Stokesove i antistokesove vrpce puno manje jakosti od Rayleighovog raspršenog zračenja, potrebno je primijeniti izvor zračenja velike jakosti. Stokesovo i antistokesovo raspršenje ovise o promjeni polarizabilnosti molekula u vremenu, pa Ramanov spektar pokazuju samo one vibracije i rotacije molekula koje mijenjaju polarizabilnost molekule. Zato u Ramanovom i infracrvenom spektru, iste vrpce obično imaju različite jakosti, a ponekad su u jednom od tih spektara potpuno nevidljive. Zato se infracrvena i Ramanova spektroskopija smatraju komplementarnima (nadopunjujući). Ramanova spektroskopija ima veliku prednost nad infracrvenom spektroskopijom jer se Ramanovi spektri mogu snimati u vodenim otopinama.
Izvori zračenja
Kao izvori zračenja, najčešće se primjenjuju laseri jer daju monokromatsko zračenje velike jakosti. Najčešće se upotrebljavaju laseri koji rade u vidljivom području, a rjeđe ultraljubičasti ili infracrveni laseri. Najčešće se primjenjuje argonski laser. Nekad su se koristile živine lampe, jer se njihovo zračenje sastoji od nekoliko linija od kojih jedna linija ima jako veliku jakost.
Optički elementi
Za Ramanovu spektroskopiju upotrebljavaju se optički elementi koji propuštaju vidljivo, ili u slučaju ultraljubičastog ili infracrvenog lasera – ultraljubičasto, odnosno infracrveno zračenje. Optički elementi su najčešće od stakla optičke kvalitete. Uzorci se stavljaju u kivete koje su slične kivetama za UV-VIS spektroskopiju.
Monokromator
Za Ramanovu spektroskopiju, upotrebljavaju se monokromatori kao i u UV-VIS spektroskopiji: optička rešetka ili optička prizma, također i izvor jake svjetlosti.
Detektor
Kao detektor, najčešće se rabi fotomultiplikator. Upotrebljavaju se i fotoosjetljive diode ili CCD čipovi.
Mikrovalna spektroskopija
Mikrovalna spektroskopija primjenjuje mikrovalno zračenje kao medij proučavanja.
Mikrovalno zračenje emitiraju i apsorbiraju rotacije molekula koje imaju dipolni moment. Mikrovalno zračenje emitiraju i apsorbiraju atomi s nesparenim elektronima u magnetskom polju, ali oni su predmet proučavanja elektronske spinske rezonancije. Mikrovalno zračenje emitiraju objekti koji imaju temperaturu svega nekollko stupnjeva iznad apolutne nule, pa se u astronomiji primjenjuje za proučavanje pozadinskog zračenja, zračenja crnog tijela samog svemira. Rotacije molekula ovise o momentu tromosti molekule, koja ovisi o njenoj geometriji. Mikrovalnom spektroskopijom se mogu odrediti geometrijski parametri. Geometrijski parametri molekule, određeni mikrovalnom spektroskopijom, smatraju se najtočnijima, jer ostale metode ne mogu postići takav stupanj preciznosti. Mikrovalnom spektroskopijom se mogu jako točno izmjeriti dipolni momenti molekula, kao i proučavati električna svojstva molekula. Mikrovalna spektroskopija se može rabiti pri identifikaciji uzoraka, ali nije toliko pogodna kao infracrvena spektroskopija ili difrakcija na polikristaliničnom uzorku, jer zahtijeva uzorak u plinskoj fazi.
Izvori zračenja
Kao izvor zračenja primjenjuje se radiofrekvencijski oscilator.
Uzorak
Uzorak je uvijek uvijek u plinskoj fazi jer molekule moraju slobodno rotirati kako bi se snimio rotacijski spektar.
Spektroskopija dalekog ultraljubičastog zračenja
Spektroskopija dalekog ultraljubičastog zračenja primjenjuje ultraljubičasto zračenje kratke valne duljine, znano kao i daleko ultraljubičasato zračenje ili vakuumsko ultraljubičasto zračenje kao medij proučavanja. Ovo zračenje uzrokuje pubuđenje elektrona u visoka energijska stanja: tzv. Rydbergove orbitale. Ova spektroskopija rabi se za proučavanje visokopobuđenih molekula. Ova spektroskopija se označava s VUV (Vacuum UltraViolet). Objekti koji emitiraju ultraljubičasto zračenje moraju biti zagrijani na ekstremno visoke temperature, pa se upotrebljava u astronomiji za proučavanje vrućih zvijezda, zvjezdanih korona i vrućih maglica.
Izvori zračenja
Izvori zračenja u dalekom ultraljubičastom području su lampe sa električnim izbojem u nekom plinu.
Optički elementi
Kao optički elementi upotrebljavaju se aluminizirana ili posrebrena zrcala. Daleko ultraljubičasto zračenje polako oštećuje metalne prevlake na zrcalima pa se one trebaju redovito obnavljati. Kako niti jedan materijal, pa čak ni zrak, ne propušta daleko ultraljubičasto zračenje, cijela aparatura se održava pod vakuumom, a uzorak se ubacuje kao plin pod niskim tlakom. Astronomski instrumenti za daleko ultraljubičasto zračenje moraju biti montirani na satelite, visoko iznad atmosfere.
Monokromator
Kao monokromatori služe optičke rešetke. Kako je teško izraditi nazubljenja rešetki veličine valne duljine dalekog ultraljubičastog zračenja, obično se rabe viši redovi difrakcije rešetke.
Detektor
Detektor je fotomultiplikator, kanalni multiplikator (channeltron).
Nuklearna magnetska rezonancija
Nuklearna magnetska rezonancija (NMR) proučava radiovalno zračenje koje interreagira s spinovima jezgara u magnetskom polju. Neke atomske jezgre imaju spin i ponašaju se kao mali magneti. U magnetkom polju se mogu orijentirati u nekoliko orijentacija koje imaju različite energije. Energije pojedinih orijentacija ovise o jačini spinskog momenta jezgre i o jakosti magnetskog polja. Apsorpcija ili emisija radiovalova mijenja orijentaciju jezgre u magnetskom polju. Elektronski omotači zasjenjuju magnetsko polje, pa svaka jezgra u atomu s različitom elektronskom strukturom, ima drukčiji odziv u NMR spektru. Jezgre osjećaju i magnetske momente susjednih jezgara, pa je iz NMR spektra moguće utvrditi i broj istovjetnih atoma u susjedstvu. Na taj način se iz NMR spektra mogu odrediti strukture molekula. Spektar se može snimati u tehnici kontinuiranog vala, gdje se primjenjuje magnetsko polje konstantnog intenziteta i promjenjiva frekvencija radiovalnog zračenja ili nepromjenjiva frekvencija i promjenjivo magnetsko polje. Moderniji instrumenti primjenjuju impulsne tehnike: Radiovalno zračenje se pusti u obliku kratkog impulsa, koji sadrži sve frekvencije, a potom se prati slobodno opadanje magnetizacije. Primjenom fourierove transformacije se dobiva NMR spektar. Ova tehnika ima prednosti jer se primjenom različitih kombinacija pulseva mogu dobiti dodatne informacije iz spektra. Za snimanje NMR spektra potrebno je odabrati kombinaciju jačine magnetskog polja i radiovalne frekvencije za jezgru svakog izotopa.
Jezgra koja se najčešće rabi je proton, jer je prisutna u mnogim organskim molekulama, i ima veliki magnetski moment.
Jezgre koje se često rabe su i 13C, 15N i 19F.
Kao referentni uzorak upotrebljava se tetrametilsilan.
Aparatura
NMR spektrometar se sastoji o velikog magneta koji stvara magnetsko polje te dviju zavojnica; jedna služi za proizvodnju uzbudnog radiovalnog zračenja, a druga služi kao detektor. Kako razlučivanje instrumenta ovisi o jakosti magnetskog polja, danas se rabe superjaki, supravodljivi magneti jakosti i 20 T]].
Elektronska spinska rezonancija
Elektronska spinska rezonancija ili elektronska paramagnetska rezonancija (ESR, EPR) proučava mikrovalno zračenje koje je emitirano ili apsorbirano od nesparenih elektrona u magnetskom polju. Spin elektronima daje magnetski moment. Spareni elektroni poništavaju svoje magnetske momente, pa elektronsku spinsku rezonanciju pokazuju samo molekule koje imaju nesparene elektrone. Elektronska spinska rezonancija funkcionira na isti način kao i nuklearna magnetska rezonancija, samo se umjesto jezgara detektiraju nespareni elektroni. Kako elektroni imaju puno veči magnetski moment od jezgara, potrebno je slabije magnetsko polje i veća frekvencija. ESR je jako osjetljiva: može detektirati vrlo niske koncentracije slobodnih radikala, manje od jedan dio na milijun.
Fotoelektronska spektroskopija
Fotoelektronska spektroskopija nije klasična spektroskopija jer ne promatra elektromagnetsko zračenje koje je molekula apsorbirala ili emitirala, već promatra elektrone koje je molekula ispustila uslijed djelovanja elektromagnetskog zračenja. Kako elekromagnetsko zračenje mora imati dovoljnu energiju za ionizaciju molekule, rabi se vakuumsko ultraljubičasto zračenje. Zračenje mora biti monokromatsko. Rjeđe se primjenjuje i rendgensko zračenje. Vakuumsko ultraljubičasto zračenje ima dovoljnu energiju za ionizaciju valentnih elektrona, pa se primjenom tog zračenja, mogu vidjeti samo ionizacije valentnih elektrona te odrediti energije njihovih orbitala. Primjenom rendgenskog zračenja, mogu se ionizirati i sržni elektroni. Primjenom rendgenskog zračenja ne može se postići razlučivanje, kao primjenom vakuumskog ultraljubičastog zračenja. Kako elektroni utječu jedni na druge, energije sržnih elektrona u manjoj mjeri ovise i o vanjskim elektronima, a tako i o elektronskom okruženju atoma. Na taj način je moguće analizirati strukture molekula. Fotoelektronska spektroskopija koja primjenjuje rendgensko zračenje, naziva se i ESCA (Electron Spectroscopy for Chemical Analysis). Fotoelektronska spektroskopija se zasniva na fotoelektričnom efektu. Energija elektrona, izbačenog iz molekule je jednaka energiji elektromagnetskog zračenja, umanjenoj za energiju vezanja elektrona koji je izbačen, te energija vibracije i rotacije molekule. U fotoelektronskom spektru se vide energije energije elektrona, a ako spektar ima dovoljno veliko razlučivanje, moguće je vidjeti i vibracijsku strukturu.
Izvori zračenja
Izvori zračenja su lampe s električnim izbojima u vodiku, dušiku ili nekom drugom, najčešće plementom, plinu. Najčešće se rabe helijeve lampe jer daju zračenje najkraće valne duljine, pa se pomoću njih mogu analizirati orbitale najniže energije. Ovisno o uvjetima rada lampe mogu se dobiti dvije spektralne linije: He I pri 21,21 eV ili He II pri 40,8 eV. U nekim uvjetima, može se primjenjivati i monokromatsko zračenje, dobiveno iz monokromatora, ali to je ograničeno na relativno male intenzitete i niske valne duljine dalekog ultraljubičastog zračenja. U novije vrijeme upotrebljavaju se i laseri koji rade u dalekom ultraljubičastom području. U rendgenskom području rabe se katodne cijevi.
Aparatura
Spektrofotometar se mora održavati u visokom vakuumu jer bi bilo kakva atmosfera apsorbirala vakuumsko ultraljubičasto zračenje i spriječila bi nesmetani prolazak elektrona prema detektoru. Uzorak, koji se mora dovesti u plinovito stanje, se propušta u vakuumsku komoru kroz malu sapnicu, tako da u komori oblikuje molekulski snop. Vakuumsko ultraljubičasto zračenje se usmjerava na molekulski snop pod pravim kutom. Elektroni, koji su emitirani iz molekulskog snopa, prolaze između para elektroda s određenim potencijalom ili kroz magnetsko polje. Zbog djelovanja električnog ili magnetskog polja, samo elektroni s točno određenom energijom mogu proći kroz elektrode ili magnet. Promjenom jakosti električnog odnosno magnetskog polja, mijenjaju se uvjeti pri kojima mogu proći elektroni različitih energija, pa se na taj način ostvaruje snimanje spektra. Detektor je kanalni multiplikator (channeltron).
Mößbauerova spektroskopija
Mößbauerova spektroskopija rabi gama zračenje kao predmet proučavanja. Gama zračenje može pobuditi atomske jezgre. Sprezanje spina jezgre s orbitalnom kutnom količinom gibanja elektrona uzrokuje cijepanje energijskih razina jezgre. Cijepanje energijskih razina je zanemarivo u usporedbi s energijskim razinama jezgre odnosno energijama gama zračenja. Mößbauerova spektroskopija rabi izvor monokromatskog gama zračenja, čije zračenje se usmjerava na uzorak. Detektorom, iza uzorka, se promatra apsorpcija gama zračenja. Mößbauerova spektroskopija upotrebljava se za ispitivanje određenih kemijskih spojeva, kristala i amorfnih tvari.
Izvor zračenja i aparatura
Kako ne postoji pogodni umjetni izvor monokromatskog gama zračenja, primjenjuje se zračenje radioaktivnih izotopa. Odabir valne duljine obavlja se promjenom valne duljine primjenom dopplerovog efekta. To se postiže postavljanjem izvora ili uzorka na pomičnu platformu. Odabiranjem relativne brzine gibanja izvora i uzorka, odabire se valna duljina.
Detektor
Kao detektori, upotrebljavaju se detektori za gama zračenje: scintilacijski brojači, Geigerov brojač i poluvodički detektori.
Ostale tehnike
Pod spektroskopske tehnike možemo ubrojiti i masenu spektrometriju, akustičku spektroskopiju, dielektričnu spektroskopiju, mehaničku spektroskopiju i radiometrijske tehnike, iako one nemaju veze s elektromagnetskim spektrom. Rezultat tih metoda je spektar (maseni spektar, spektar zvučnih valova, spektar frekvencija električnog polja, spektar frekvencija mehaničkog naprezanja, spektar , , , zračenja...), pa ih uvjetno možemo ubrojiti u spektroskopiju.
Izvori
Vanjske poveznice
- Ostali projekti


