Larmorova precesija

Larmorova precesija određuje frekvenciju precesije elektrona u vanjskom magnetskom polju, a odredio ju je 1897. J. Larmor. [1]
Larmorova precesija i dijamagnetizam
O djelovanju magnetskog polja na atome daje vrlo dobar uvid osnovni teorem koji je našao J. Larmor. U atomima izvode elektroni vrlo brza periodična gibanja oko svoje jezgre. Kad ukopčamo magnetsko polje, tad po Larmoru čitav elektronski sustav zadobije jednoliku vrtnju (rotaciju) oko smjera magnetskog polja. Ova pridošla precesija neovisna je o specijalnoj strukturi atoma.
Larmorov teorem dokazat ćemo na jednostavnom primjeru da se elektron u kružnici vrti oko težišta atoma. Brzina elektrona u kružnici jednaka je r∙ω0, gdje je ω0 kutna brzina, a ubrzanje ν/r = r∙ω2. Sa F označit ćemo silu koja drži elektron u atomu. Newtonov zakon gibanja, specijaliziran za vrtnju glasi:
Na elektron sada neka djeluje i magnetsko polje koje stoji okomito na ravninu gibanja elektrona. Njegova sila stoji okomito na brzinu elektrona. Pod djelovanjem tih dviju centralno orijentiranih sila elektron će se opet kretati u kružnici, ali s drugom brzinom. Novu kutnu brzinu označit ćemo sa ω. Zakon gibanja glasi:
Za silu magnetskog polja uzeli smo suprotan predznak, jer ona za pozitivno nabijenu česticu, koja se vrti u pozitivno određenom smjeru, ima smjer suprotan od sile F. Promjenu frekvencije označit ćemo sa ωL:
Uvrstimo li to u jednadžbu gibanja, dobivamo:
Ovdje se ukida prvi član lijeve strane s prvim članom desne strane jednadžbe. Vanjsko magnetsko polje izaziva malu smetnju u atomskom sustavu. Promjena frekvencije bit će mala. Prema tome možemo zanemariti član sa ωL2 i član sa ωL∙H. Za promjenu kutne brzine dobivamo:
Ovo je Larmorova jednadžba za promjenu kutne brzine, izazvanu vanjskim magnetskim poljem. Kutna brzina ω jednaka je 2∙π∙ν. Za promjenu frekvencije u magnetskom polju dobivamo time:
Bez obzira na to da li se elektroni vrte u velikim ili malim kružnicama, oni jednako mijenjaju u magnetskom polju svoju frekvenciju. Djelovanjem magnetskog polja sustav elektrona zadobije jednoliku vrtnju oko magnetskih silnica. Budući da je električni naboj elektrona negativan, ta inducirana vrtnja ide u pozitivno određenom smjeru.
Ovdje nam se nameće pitanje: Kako može magnetsko polje ubrzati ili usporiti vrtnju elektrona kad uvijek djeluje okomito na smjer vrtnje? Ovaj paradoks razjašnjuje se u elektrodinamici. Pri ukopčavanju magnetskog polja javlja se i električno polje i ono uzrokuje Larmorova ubrzanja. Kad magnetsko polje postane konstantno, električno polje opet iščezava.
Larmorovom precesijom mijenjaju se impulsi vrtnje atoma, a time ujedno i njihovi magnetski momenti. Izračunat ćemo koliko ta promjena impulsa vrtnje iznosi za elektron koji kruži u ravnini okomitoj na smjer magnetskog polja. Prije ukopčavanja magnetskog polja elektron ima impuls vrtnje:
U magnetskom polju mijenja se kutna brzina za Larmorovu veličinu ωL, pa promjena impulsa vrtnje iznosi:
Toliki bi impuls vrtnje magnetsko polje induciralo svim elektronskim stazama kojima je os paralelna sa smjerom polja. Međutim, ravnina vrtnje elektrona može stajati u bilo kojem smjeru prema magnetskim silnicama. Prema tome, moramo u gornjem izrazu mjesto r2 uzeti neku srednju vrijednost. Kvadrat udaljenosti elektrona od jezgre jednak je:
Ako ravnina gibanja elektrona stoji okomito na smjer magnetskog polja, tad je r2 jednak x2 + y2. Očito mora umjesto r2 u zadnjoj jednadžbi stajati srednja vrijednost od x2 + y2. Kod slučajno razbacanih radijvektora po svim smjerovima srednja je vrijednost od x2 jednaka 1/3∙r2. Dakle:
Za prosječni inducirani impuls vrtnje dobivamo, prema tome, izraz:
S promjenom impulsa vrtnje vezana je i promjena magnetskog momenta. Općenito postoji između magnetskog momenta i impulsa vrtnje odnos:
Uvrstimo li ovdje Larmorovu kutnu brzinu, dobivamo:
Odatle možemo lako proračunati polarizaciju ili magnetski moment jedinice volumena. U 1 m3 neka je N atoma. Svaki atom ima Z elektrona. Z je redni broj elementa. Za r2 moramo staviti prosječnu vrijednost svih elektrona u atomu. Magnetska polarizacija jednaka je:
Magnetska susceptibilnost odatle je jednaka:
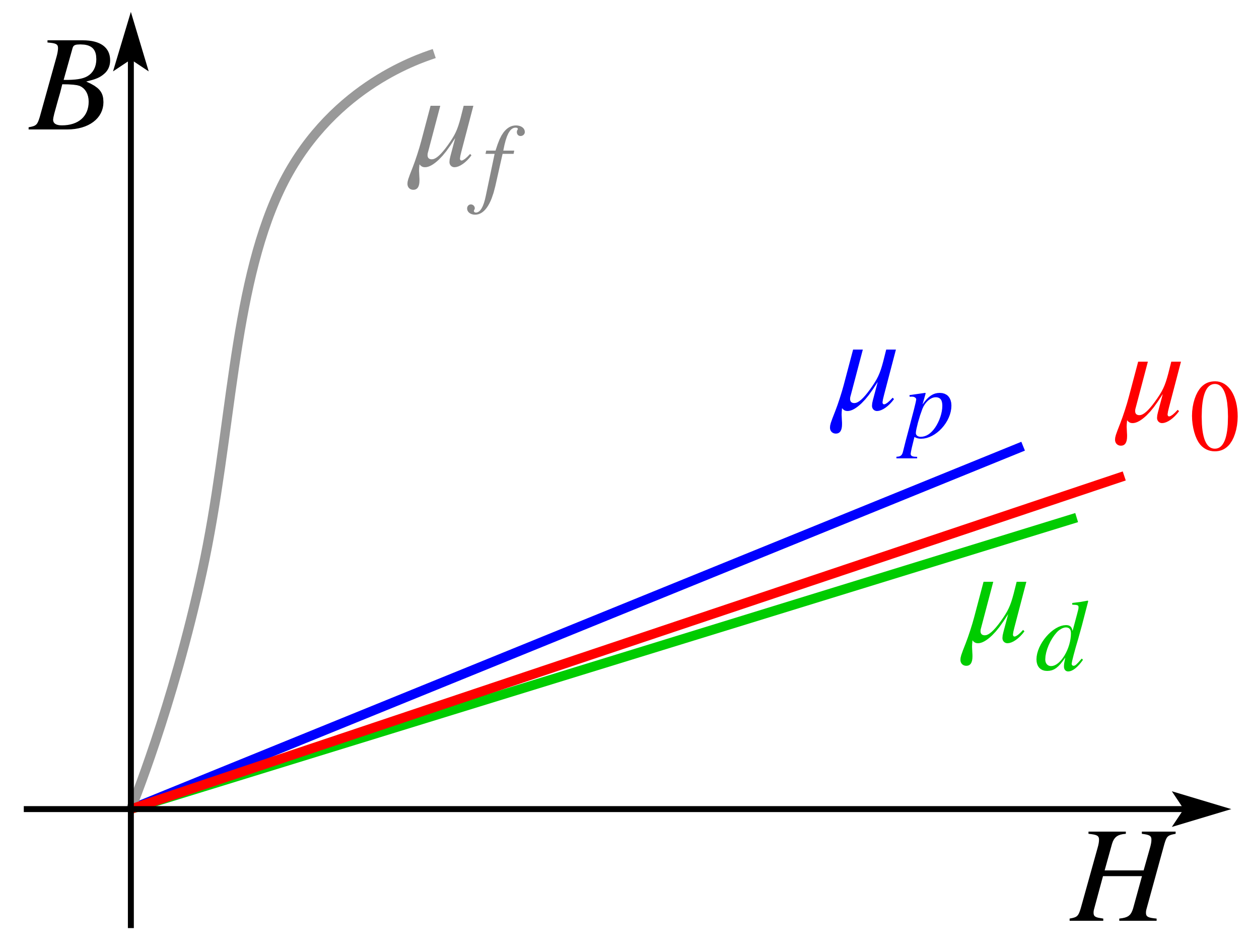
Inducirana polarizacija ima pozitivan smjer od smjera magnetskog polja. Magnetska susceptibilnost je negativna. Odatle vidimo, da je dijamagnetizam opće svojstvo svih atoma. U tvarima, koje se ponašaju paramagnetski dijamagnetičnost je zastrta paramagnetizmom, koji potječe od stalnih (permanentnih) magneta.
Mjesto da računamo s polarizacijom po m2 možemo računati i s polarizacijom po gramu. N u gornjoj jednadžbi tada nam znači broj atoma po gramu. Ako sa A označimo atomsku težinu elementa, tad je broj atoma u 1 g dan omjerom između Avogadrovog broja L i atomske težine. Magnetska susceptibilnost po gramu iznosi, dakle:
Za sve elemente je omjer između Z i A približno 1/2. Polumjer atoma je prosječno velik 10-10 m. L/6 jednako je 1023. Veličina e2/(m∙c2), takozvani klasični polumjer elektrona, iznosi 2,8∙10-15 m. Prema tome dobivamo da je magnetska susceptibilnost po gramu reda veličine 10-6. To se vrlo dobro slaže s iskustvom.
Na osnovu teoretskog izraza za dijamagnetičku susceptibilnost možemo izračunati promjer atoma. Ta nova metoda stoji u suglasju s ostalim određivanjima veličine atoma. Prema elementima s najvišim rednim brojem postaje prosječni polumjer sve manji, što znači da su elektroni bliže privučeni atomskoj jezgri.
| Kemijski element | Z | A | ζg/10-6 | r2 = - 3,5∙10-11∙A/Z∙ζg |
|---|---|---|---|---|
| Klor | 17 | 35,5 | -0,6 | 4∙10-18 cm2 |
| Brom | 35 | 80 | -0,4 | 3∙10-18 cm2 |
| Živa | 80 | 200 | -0,2 | 2∙10-18 cm2 |
| Bizmut | 83 | 209 | -1,2 | 90∙10-18 cm2 |
Za bizmut dobiva se prevelik polumjer atoma. To odstupanje od klasične jednadžbe za susceptibilnost objasnila je kvantna teorija. [2]
Izvori
- ↑ Larmor , Joseph, [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2019.
- ↑ Ivan Supek: "Nova fizika", Školska knjiga Zagreb, 1966.















