Topljivost: razlika između inačica
Bot: Automatski unos stranica |
m file->datoteka |
||
| Redak 1: | Redak 1: | ||
<!--'''Topljivost'''-->[[ | <!--'''Topljivost'''-->[[Datoteka:Potassium-permanganate-solution cropped.png|mini|600px|Otopina kalijeva permanganata]] | ||
'''Topljivost''' je svojstvo tvari da s drugom tvari tvori homogenu smjesu. Najčešće je otapalo kapljevina, dok otopljena tvar može biti čvrsta, kapljevita ili plinovita. | '''Topljivost''' je svojstvo tvari da s drugom tvari tvori homogenu smjesu. Najčešće je otapalo kapljevina, dok otopljena tvar može biti čvrsta, kapljevita ili plinovita. | ||
<ref name="Top">[http://www.enciklopedija.hr/Natuknica.aspx?ID=61798] Leksikografski zavod Miroslav Krleža, Hrvatska enciklopedija: Topljivost</ref> | <ref name="Top">[http://www.enciklopedija.hr/Natuknica.aspx?ID=61798] Leksikografski zavod Miroslav Krleža, Hrvatska enciklopedija: Topljivost</ref> | ||
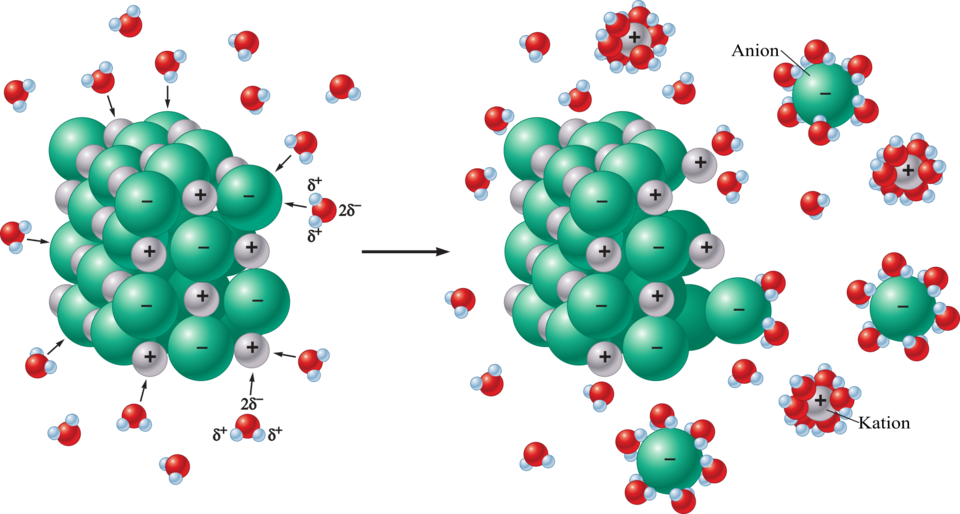
[[ | [[Datoteka:Dysocjacja w wodzie.png|mini|600px|Otapanje kristala u vodi: disocijacija i hidratacija]] | ||
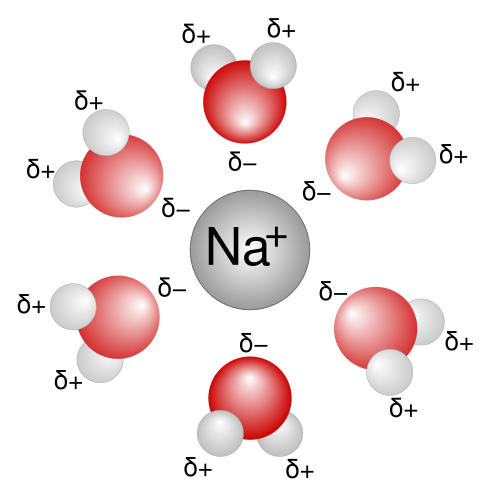
[[ | [[Datoteka:Na+H2O.svg|mini|350px|Hidratacija iona natrija]] | ||
:*Topljivost se obično definira kao masa otopljene tvari na 100 g otapala (vode) pri 20°C. | :*Topljivost se obično definira kao masa otopljene tvari na 100 g otapala (vode) pri 20°C. | ||
| Redak 48: | Redak 48: | ||
</table> | </table> | ||
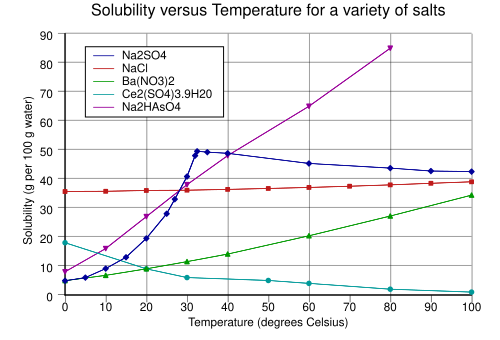
[[ | [[Datoteka:SolubilityVsTemperature.svg|mini|450px|right|Dijagram topljivosti nekih soli u vodi ovisno o temperaturi]] | ||
==Ovisnost topljivosti o temperaturi== | ==Ovisnost topljivosti o temperaturi== | ||
Topljivost tvari može za različite tvari biti vrlo različita (netopljive, slabo topljive, dobro topljive tvari), a redovito se mijenja s temperaturom: s porastom temperature najčešće se povećava, ali se može i smanjivati ili se u jednom temperaturnom intervalu povećavati, a u drugome smanjivati (dijagram). | Topljivost tvari može za različite tvari biti vrlo različita (netopljive, slabo topljive, dobro topljive tvari), a redovito se mijenja s temperaturom: s porastom temperature najčešće se povećava, ali se može i smanjivati ili se u jednom temperaturnom intervalu povećavati, a u drugome smanjivati (dijagram). | ||
Posljednja izmjena od 13. svibanj 2022. u 03:01

Topljivost je svojstvo tvari da s drugom tvari tvori homogenu smjesu. Najčešće je otapalo kapljevina, dok otopljena tvar može biti čvrsta, kapljevita ili plinovita. [1]
- Topljivost se obično definira kao masa otopljene tvari na 100 g otapala (vode) pri 20°C.
O čemu ovisi topljivost
Topljivost tvari ovisi o međumolekulskim silama između otapala i otopljene tvari, odn. o energetskim promjenama tijekom otapanja.
Treba razlikovati dva dijela procesa otapanja. Prvi dio procesa otapanja je energija potrebna da se kruta tvar disocira, odnosno da se tvar razdvoji na slobodne ione (ionske tvari) ili slobodne molekule (kovalentne tvari). Taj dio procesa otapanja traži ulaganje energije, on je endoterman jer je potrebno razbiti određenu kristalnu strukturu krute tvari koju otapamo. Drugi dio procesa otapanja je energija koja se oslobađa jer kod slobodnih ionskih čestica dolazi do hidratacije, vezivanja s molekulama vode (ion-dipol veza), odnosno kod slobodnih molekula dolazi do solvatacije, vezivanja s molekulama nekog nepolarnog otapala (veza inducirani dipol-inducirani dipol). Taj drugi dio procesa otapanja oslobađa energiju, jer su hidratacija i solvatacija egzotermni procesi. U konačnici je proces otapanja endoterman ako je energija disocijacije veća od energije hidratacije, odnosno proces otapanja je egzoterman ako je energija disocijacije manja od energije hidratacije. Slično vrijedi za kovalentne tvari koje se dobro otapaju u nepolarnim otapalima i gdje je hidratacija zamijenjena solvatacijom.[2]
Utjecaj polarnosti otapala na topljivost neke tvari najčešće se opisuje pravilom prema kojemu slično otapa slično, što znači da će se polarne tvari najbolje otapati u polarnim otapalima, a nepolarne u nepolarnima, iako to pravilo nije uvijek primjenljivo. Temperatura i tlak utječu na ravnotežu otapanja. S porastom temperature topljivost čvrstih tvari najčešće se povećava, dok plinovi postaju slabije topljivi u vodi, ali bolje topljivi u organskim otapalima. Topljivost plinova proporcionalna je tlaku plina (Henryjev zakon). Brzina otapanja ovisi o veličini čestica, jer se otapanje zbiva samo na površini čestice, pa se manje čestice otapaju brže, jer imaju veću specifičnu površinu. Brzina otapanja također ovisi o miješanju (koje ubrzava otapanje), količini već otopljene tvari (približavanjem koncentracije maksimalnoj topljivosti otapanje se usporava) i temperaturi, koja uz povećanje maksimalne topljivosti povećava i brzinu otapanja.[1]
Podjela tvari i otopina prema topljivosti
Tvari se otapanjem mogu međusobno miješati u svim omjerima (primjerice etanol i voda), u ograničenim omjerima ili u zanemarivim omjerima, kada se smatraju netopljivima. Otopina koja sadrži maksimalnu ravnotežnu količinu otopljene tvari pri danim uvjetima naziva se zasićenom otopinom. Pri određenim uvjetima količina otopljene tvari može biti nešto veća od ravnotežne, a nastala metastabilna otopina naziva se prezasićenom.
Postoje i čvrste otopine, homogene smjese čvrstih tvari (npr. slitine, staklo).
Količina otopljene tvari se najčešće izražava kao množinska ili masena koncentracija, ili pak kao množinski ili maseni udio otopljene tvari u otapalu.
Topljivost u vodi prema vrsti kemijske veze
| Vrsta veze | Topljivost tvari u vodi | Primjer |
|---|---|---|
| ionska | uglavnom topljive | vidi ispod |
| metalna | netopljive | Fe |
| osim ako reagiraju s vodom | K | |
| polarna kovalentna | topljive ako tvore vodikovu vezu | glukoza |
| topljive ako reagiraju s vodom | HCl | |
| inače netopljive | eter | |
| nepolarna kovalentna | uglavnom netopljive | benzen |
| neke slabo topljive | O2 | |
| kovalentna u kristalu | netopljive | dijamant |
Topljivost ionskih spojeva u vodi
| Topljive soli | Netopljive soli |
|---|---|
| sve soli alkalijskih metala i NH4+ | karbonati (osim alkalijskih metala i NH4+) |
| nitrati | sulfiti (osim alkalijskih metala i NH4+) |
| acetati | fosfati (osim alkalijskih metala i NH4+) |
| kloridi, bromidi i jodidi (osim Ag+, Pb2+, Cu+ i Hg22+) | hidroksidi i oksidi (osim alkalijskih metala, NH4+, Ba2+, Sr2+, Ca2+ i Tl+) |
| sulfati (osim Ag+, Pb2+, Ba2+, Sr2+ i Ca2+) | sulfidi (osim alkalijskih i zemnoalkalijskih metala te NH4+) |
Ovisnost topljivosti o temperaturi
Topljivost tvari može za različite tvari biti vrlo različita (netopljive, slabo topljive, dobro topljive tvari), a redovito se mijenja s temperaturom: s porastom temperature najčešće se povećava, ali se može i smanjivati ili se u jednom temperaturnom intervalu povećavati, a u drugome smanjivati (dijagram).
Topljivost tvari u otapalima
Voda je uobičajeno ali istovremeno vrlo osobito otapalo. Molekule vode su dipoli među kojima djeluje vodikova veza te je voda najpolarnije otapalo. Neka druga otapala su također polarna (alkoholi), slabo polarna (eteri) ili nepolarna (ugljikovodici). U vodi se zato dobro otapaju polarne odnosno ionske tvari, građene od nabijenih čestica iona a to su razne soli, kiseline, hidroksidi, dok se nepolarne tvari (jod, sumpor) ne otapaju ili ne miješaju (ugljikovodici, ulja). Obrnuto u nepolarnim ili slabo polarnim otapalima (ugljikovodici, eteri) slabo se otapaju ionske tvari a dobro se otapaju nepolarne kovalentne tvari (ulja, masti). Zato je postavljeno "zlatno pravilo" otapanja:
"Slično se otapa u sličnom!" [2]
Također vrijedi opčenito: topljivost krutih tvari raste porastom temperature otapala dok topljivost plinova pada.