Nikotinamid adenin dinukleotid
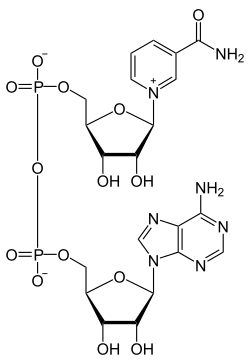
Nikotinamid adenin dinukleotid (NAD +) je koenzim prisutan u svim živim stanicama Ovaj je spoj dinukleotid, jer se sastoji od dva nukleotida spojena putem fosfatnih grupa. Jedan nukleotid sadrži adeninsku bazu, a drugi nikotinamid.[1]
U metabolizmu, NAD + sudjeluje u redoks reakcijama, prenoseći elektrone s jedne reakcije do druge. Koenzim se, stoga u stanicama pojavljuje u dva oblika, NAD + kao oksidirajući agens prima elektrone s druge molekule i postaje reduciran. Ta reakcija formira NADH, koji se zatim može koristiti kao reducirajući agens (doniranje elektrona). Reakcije elektronskog prijenosa su glavna funkcija NAD +. Međutim, on se također koristi u drugim staničnim procesima, najznačajniji od kojih su oni u kojima je on supstrat enzima koji dodaju ili uklanjaju kemijske grupe s proteina, u posttranslacijskim modifikacijama. Zbog značaja tih funkcija, enzimi koji sudjeluju u metabolizmu NAD+ meta su u otkrivanju novih lijekova.
U organizmu,NAD+ može biti sintetiziran iz jednostavnih gradivnih blokova, kao sinteza „ex novo“ iz aminokiseline triptofana ili asparaginske kiseline. U alternativi, kompleksnije se komponente koenzima uzimaju iz hrane kao vitamin pod nazivom niacin. Slični spojevi nastaju u reakcijama kojima se razgrađuje NAD+ struktura. Te gotove komponente zatim prolaze kroz put spasenja nukleotida koji ih recirkulira u aktivni oblik. Dio NAD+ sadržaja se također pretvara u nikotinamid adenin dinukleotid fosfat (NADP+) ; kemija tog srodnog koenzima je slična s NAD+- om, ali podliježe različitim pravilima u metabolizmu.
Fizička i kemijska svojstva
Nikotinamid adenin dinukleotid, poput svih dinukleotida , sastoji se od dva nukleotida vezana parom premoštenih fosfatnih skupina. Nukleotidi se sastoje od riboznih prstenova, jedan s adeninom vezanim za prvi atom ugljika (1 ' pozicija), a drugi s nikotinamidom u toj poziciji. Nikotinamidna skupina može biti vezana u dvije orijentacije za taj anomerni ugljik. Zbog te dvije moguće strukture, spoj postoji kao dva diastereomera. β – nikotinamidni NAD+ diastereomer je nađen u organizmima. Ti nukleotidi su međusobno spojeni mostom između dvije fosfat ne grupe preko 5 ' ugljika. [2]

U metabolizmu, spoj prima ili donira elektrone u redoks reakcijama.[3] Takve reakcije (sažete u donjoj formuli) obuhvaćaju uklanjanje dva atoma vodika s reaktanta -R), u obliku hidridnog iona (H-), i protona (H+). Proton se oslobađa u otopinu, dok se reduktant RH 2 oksidira i NAD+ se reducira u NADH transferom hidrida do nikotinamidnog prstena.
RH 2 +NAD+→ NADH + H+ + R
S hidridnog elektronskog para, jedan elektron se prenosi do pozitivno naelektriziranog dušika u nikotinamidnom prstenu, a drugi atom vodika se presi do -C4 ugljika nasuprot tom dušiku. Potencijal NAD+/ NADH redoks para je -0.32 volt i, što čini NADH jakim redukujućim faktorom.[4] Reakcija je lako reverzibilna, pri čemu NADH reducira druge molekule i reoksidira se do NAD +. To znači da koenzim može kontinuirano cirkulirati između NAD + i NADH oblika bez gubitka. [2]
Reference
- ↑ Nelson DL; Cox MM (2004). Lehninger Principles of Biochemistry (4th ed.). W. H. Freeman. ISBN 0-7167-4339-6.
- ↑ 2,0 2,1 • Nepoznat parametar:
coauthors
• Nepoznat parametar:PMID
• Nepoznat parametar:pmc
• Nepoznat parametar:issue
• Parametartypenije dopušten u klasijournal
• Parametarurlnije dopušten u klasijournal - ↑ • Nepoznat parametar:
coauthors
• Nepoznat parametar:PMID
• Nepoznat parametar:Doi
• Nepoznat parametar:Volume
• Nepoznat parametar:issue
• Parametartypenije dopušten u klasijournal
• Parametarformatnije dopušten u klasijournal
• Parametarurlnije dopušten u klasijournal
• Parametaraccessdatenije dopušten u klasijournal - ↑ • Nepoznat parametar:
coauthors
• Nepoznat parametar:PMID
• Nepoznat parametar:issue
• Parametartypenije dopušten u klasijournal
Literatura
coauthors• Nepoznat parametar:
refrefrefPovijest
ref, A history of early enzymology.
ref, A textbook from the 19th century.