Faradayevi zakoni elektrolize
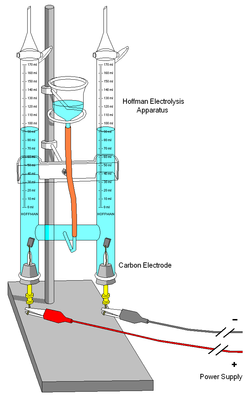
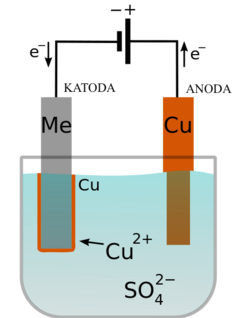
Faradayevi zakoni elektrolize su dva fizikalna zakona kojima je M. Faraday opisao proces elektrolize. Prema prvom zakonu elektrolize, masa tvari nataložena na elektrodi pri elektrolizi razmjerna je umnošku kostantne električne struje i vremena u kojem je ona tekla kroz elektrolit. Prema drugom zakonu masa različitih tvari nataložena na elektrodi pri elektrolizi razmjerna je količniku molarne mase i električnoga naboja iona tvari. Zakoni se mogu izraziti jednom jednadžbom:
gdje je: m - masa nataložene tvari (g), M - molarna masa (g/mol), I - jačina električne struje (A), t - vrijeme protjecanja električne struje (s), e - elementarni električni naboj (1,602 176 487·10−19 C), NA - Avogadrova konstanta (6,0221412 x 1023 mol-1), z - valencija iona tvari. [1]
Prvi Faradeyev zakon elektrolize
Između količine elektriciteta koja je protekla kroz elektrolit i količine izlučenih kemijske tvari postoji odnos koji je ustanovio Faraday 1832. On je utvrdio da dvaput jača struja izluči u isto vrijeme na katodi dvaput više vodika ili neke kovine, a isto tako da u dvaput duljem vremenu izluči dvaput veću količinu tvari. Prema tome prvi Faradeyev zakon elektrolize glasi: Množina izlučenog elektrolita razmjerna je s umnoškom jakosti električne struje i vremena, to jest s količinom proteklog elektriciteta, pa je:
kako je:
onda dobivamo:
gdje je: m - količina izlučenog elektrolita u kilogramima, Q - količina proteklog elektriciteta u As (As = C), I - jakost električne struje u amperima, t - vrijeme u sekundama, a - elektrokemijski ekvivalent odgovarajuće tvari. Elektrokemijski ekvivalent je ona količina tvari izražena u kilogramima koju izluči jedan kulon odnosno 1 As elektriciteta.
Drugi Faradeyev zakon elektrolize
Drugi Faradeyev zakon elektrolize govori kako se odnose količine različitih tvari koje izluči ista količina elektriciteta iz različitih elektrolita, odnosno ista jakost struje u isto vrijeme. Taj zakon glasi: Količine različitih tvari, izlučenih istom jakosti električne struje i u isto vrijeme, odnose se kao ekvivalentne mase dotičnih tvari.
Ekvivalentna masa je omjer između atomske mase A i valencije z neke tvari, to jest:
Označimo li s m1 izlučenu količinu jednog elektrolita, a sa m2 drugoga, i ako su A1/z1 i A2/z2 pripadne ekvivalentne mase, možemo drugi Faradeyev zakon matematički izraziti i ovako:
Budući da je prema prvom Faradeyevom zakonu m1 = a1∙I∙t i m2 = a2∙I∙t, prelazi taj razmjer u:
Elektrokemijski ekvivalenti odnose se isto tako kao i ekvivalentne mase odgovarajućih kemijskih tvari.
Pomoću prvog Faradeyovog zakona može se odrediti količina elektriciteta Q tako da se mjeri količina izlučenog elektrolita m uz poznati elektrokemijski ekvivalent a odgovarajuće tvari. Na tome se zasnivaju kulometri ili mjerni instrumenti za mjerenje količine elektriciteta. Tako se na primjer kulometar s praskavcem osniva na mjerenju količina plina praskavca, koji se javlja pri elektrolizi vode. Praskavac je eksplozivna smjesa kisika i vodika. Električna struja jaka 1 amper izluči u 1 minuti 10,5 cm3 plina praskavca (7 cm3 vodika i 3,5 cm3 kisika) kod tlaka 1 bar i 0 °C. Kulometar sa srebrom je vrlo precizan i služi za određivanje kulona, a prema tome i ampera. Kao elektrolit služi vodena otopina srebrnog nitrata, a anoda je od čistog srebra. Platinska posuda služi kao katoda i ona se važe prije i poslije elektrolize i tako se ustanovi količina izlučenog srebra. Električna struja jaka 1 amper izluči u 1 sekundi iz otopine srebrnog nitrata 1,118 ∙ 10-6 kg (1,118 mg) srebra.
Pitanje je sada kolika je količina električne struje potrebna da se izluči kilogram - ekvivalent odgovarajuće tvari. Pri tom moramo reći da je gramatom onolika količina tvari u gramima kolika je njena atomska masa A. Iz toga proizlazi da je kilogramatom = 103 gramatoma. Odnosno:
- 1 kilogramatom = A kg
Pokusi su pokazali da je za izlučivanje 1 kilogramekvivalenta potrebna količina elektriciteta od 9,65 ∙107 ampersekundi. taj se broj zove Faradeyeva konstanta i označuje se s F.
Valencija nekog kemijskog elementa je broj atoma vodika s kojim se može spojiti 1 atom nekog elementa: [2]
- 1 kilogram ekvivalent = 1 kilomol / valencija






