Arnold Sommerfeld
| Arnold Sommerfeld | |
 | |
| Rođenje | 5. prosinca 1868. Kalinjingrad, Rusija |
|---|---|
| Smrt | 26. travnja 1951. München, Njemačka |
| Državljanstvo | Nijemac |
| Polje | Fizika |
| Institucija | Sveučilište u Göttingenu Sveučilište u Clausthal-Zellerfeldu, Sveučilište u Aachenu Sveučilište u Münchenu |
| Alma mater | Sveučilište u Kalinjingradu |
| Akademski mentor | Ferdinand Lindemann |
| Poznat po | Konstanta fine strukture Bohrov model atoma Kvantni brojevi Sommerfeldova metoda polinoma |
| Istaknute nagrade | Matteuccijeva medalja (1924.) Član Kraljevskog društva (od 1926.) |
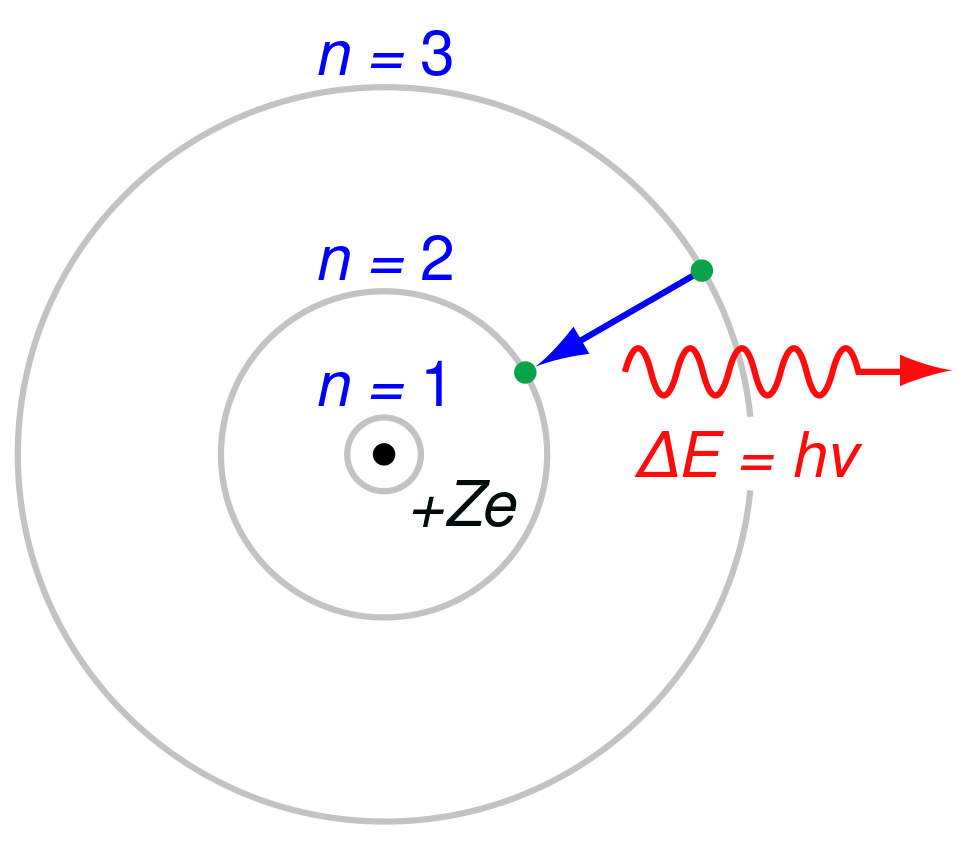

Arnold Sommerfeld (Königsberg, danas Kalinjingrad, 5. prosinca 1868. – München, 26. travnja 1951.), njemački fizičar i matematičar. Studirao matematiku i fiziku u Königsbergu, doktorirao 1891. Karijeru započeo na Sveučilištu u Göttingenu 1895. Bio je pročelnik Odjela za primijenjenu mehaniku na Sveučilištu u Aachenu (od 1900. do 1906.), kao izvanredni profesor predavao je i istraživao hidrodinamiku, a od 1906. bio je redoviti profesor i direktor novog Instituta za teorijsku fiziku u Münchenu. Više od 32 godine u Münchenu predavao mehaniku, mehaniku elastičnih sredstava, elektrodinamiku, optiku, termodinamiku, statističku mehaniku, te parcijalne diferencijalne jednadžbe. Priredio je glasovita Predavanja iz teorijske fizike (njem. Vorlesungen über theoretische Physik, u 6 sv., 1943. – 1953.). Među prvim znanstvenicima u Europi prihvatio je i poopćio Bohrov model atoma, uključivši specijalnu relativnost i eliptične staze. Primjenom novih pravila kvantizacije uveo je tri kvantna broja (nr - radijalni kvantni broj, nφ - kvantni broj kutne količine gibanja, nr + nφ = n - glavni kvantni broj koji odgovara Bohrovu cijelom broju). Njegov je rad urodio uvođenjem bezdimenzijske konstante fine strukture (1915.) u atomsku i kvantnu fiziku. Sommerfeldov udžbenik Građa atoma i spektralne linije (njem. Atombau und Spektrallinien, 1916.) temelj je razvoja kvantne mehanike. Imao je dar za otkrivanje i razvoj talenata u fizici: četiri njegova doktoranda (W. K. Heisenberg, W. Pauli, P. Debye i H. A. Bethe) i dvojica poslijediplomskih studenata (L. C. Pauling i I. I. Rabi) dobili su Nobelove nagrade. Za fundamentalne doprinose u atomskoj te doprinose kvantnoj fizici i razvoju moderne teorijske fizike, primio je Lorentzovu, Planckovu i Ørstedovu medalju; bio je član Kraljevskog društva (eng. Royal Society) od 1926., te američke, sovjetske i indijske akademije. [1]
Doprinosi
Konstanta fine strukture
Konstanta fine strukture (oznaka α) je prirodna konstanta, bezdimenzionalna veličina u fizici elementarnih čestica koja opisuje jakost međudjelovanja između električkih nabijenih čestica i fotona. Ona je konstanta vezanja u elektromagnetskim djelovanjima, a određuje finu strukturu (cijepanje spin–staza) u atomskim spektrima. Njezina su definicija i vrijednost:
gdje je:
- e - elementarni naboj;
- ħ = h/2π - reducirana Planckova konstanta;
- c - brzina svjetlosti u vakuumu;
- ε0 - dielektrična permitivnost vakuuma.
Konstantu fine strukture u fiziku je uveo A. Sommerfeld, proširujući Bohrov model atoma uključivanjem relativističkih pojava i eliptičnih staza gibanja elektrona, te kvantizirajući energiju, linearnu i kutnu količinu gibanja. Konstanta fine strukture je važna u teorijskim proračunima i razumijevanju elektromagnetskih međudjelovanja i zračenja te ulazi u matrične elemente različitih elektromagnetskih procesa, određujući njihove udarne presjeke i raspade.[2]
Kvantni broj
Kvantni broj je broj koji opisuju kvantnomehaničko stanje elektrona u atomu, nukleona u atomskoj jezgri i subatomskih čestica (kvark, lepton i čestice prijenosnice polja temeljnih djelovanja). Kvant i kvantni broj u fiziku je uveo M. Planck 1900. kako bi objasnio zračenje crnoga tijela i slaganje teorije crnoga tijela s pokusima. U modernoj fizici pod pojmom kvantizacije podrazumijeva se prijelaz iz zakonitosti klasične fizike u kvantnu mehaniku. Kvantiziranje gravitacije jedan je od najvećih problema suvremene fizike elementarnih čestica i kozmologije.
Tipično je značenje kvantnih brojeva stanjâ elektrona u atomu sljedeće:
- glavni kvantni broj n određuje svojstvene vrijednosti energije elektrona,
- orbitalni kvantni broj l određuje vrijednost kutne količine gibanja elektrona u kvantnim stazama,
- magnetski kvantni broj m određuje moguće orijentacije kutne količine gibanja u odnosu na os vanjskoga magnetskoga polja,
- a kvantni broj spina s određuje spinsku kutnu količinu gibanja elektrona.
Ukupni broj različitih stanja u atomu za kvantne brojeve n, l i m iznosi (2 l + 1), a zbog dviju spinskih orijentacija (projekcija) na vanjsku os taj se broj udvostručuje. Stanja elektrona u modelu Fermijeva plina opisana su samo glavnim kvantnim brojem n i s dvije orijentacije spina. Kvanti svjetlosti (foton), kao bozoni cjelobrojnoga spina opisani su Bose-Einsteinovom statistikom, a istoj statistici podvrgavaju se i kvanti titranja kristalne rešetke (fonon) kao bozoni nultoga spina. Neutroni i protoni, šire hadroni, uz kvantni broj spina imaju još i kvantni broj izospina. Uz spin i okus (gornji, donji, strani …), kvarkovi nose i kvantni broj jakoga naboja, koji se uobičajeno naziva bojom (crvena, zelena, plava), a antikvarkovi odgovarajuću antiboju. Teorija polja boje u kvantnome obliku poznata je kao kvantna kromodinamika.[3]
Izvori
- ↑ Sommerfeld, Arnold, [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2016.
- ↑ konstanta fine strukture, [2] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2016.
- ↑ kvantni broj, [3] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2016.
