John Dalton
| John Dalton | |
 | |
| Rođenje | 6.rujna 1766. Eaglesfield, Cumbria, Ujedinjeno Kraljevstvo |
|---|---|
| Smrt | 27. srpnja 1844. Manchester, Greater Manchester, Ujedinjeno Kraljevstvo |
| Narodnost | Englez |
| Polje | Kemija, fizika |
| Poznat po | Daltonova atomska teorija, Daltonov zakon, Daltonizam Relativna atomska masa |
| Istaknute nagrade | Član Kraljevskog društva (1826.) |

John Dalton (Eaglesfield, 6. rujna 1766. - Manchester, 27. srpnja 1844.), engleski prirodoslovac, kemičar i fizičar. Zbog doprinosa razvoju atomske teorije smatra se jednim od utemeljitelja suvremenoga prirodoslovlja. U knjizi Novi sustav kemijske filozofije (eng. New System of Chemical Philosophy, I, 1808., II, 1810.) pretpostavio je da se kemijski elementi sastoje od malih neuništivih čestica, atoma. Time je utemeljio atomsku teoriju građe tvari, ustvrdivši da se svaki kemijski element sastoji od atoma iste vrste, dok se kemijski spojevi sastoje od različitih atoma. Uveo je posebne simbole za kemijske elemente i spojeve i dao pregled relativnih atomskih masa. Proučavajući zakonitosti kemijskog spajanja, 1802. otkrio zakon umnoženih masenih omjera, a 1807. i zakon parcijalnih tlakova (Daltonov zakon).
Osim kemijom, bavio se sustavnim meteorološkim istraživanjima. Kako je bio slijep za boje, proučavao je tu anomaliju, koja je po njemu nazvana daltonizam. Premda su se neki Daltonovi zaključci pokazali pogrešnima (na primjer predodžba o nedjeljivosti atoma, koja je pobijena otkrićem radioaktivnoga raspada), njegova atomska teorija i predodžba o atomskim masama elemenata imaju ogromno značenje za razvoj fizike i kemije.[1]
Životopis
Dalton je u školi bio marljiv i uporan učenik, vješt u računanju. Kad je smrću učitelja škola zatvorena, Dalton je sa 18 godina otvorio svoju školu u napuštenu sjeniku, a zatim u Domu kvekera. Prvo se bavio meteorologijom, a zatim kemijom. Učio je i podučavao, osim matematike i fizike, englesku gramatiku, grčki, latinski i francuski jezik. S 22 godine razmišljao je o studiranju prava ili medicine, no zbog nepodržavanja obitelji te zbog činjenice da je neistomišljenicima studiranje ili predavanje na engleskim fakultetima bili zabranjeno ipak nije, te je 1793. otišao u Manchester.
Godine 1803. predložio je svoje principe atomske teorije (uveo je pojam atomske težine, točnije, relativne atomske mase, uzevši kao standard atom vodika (H), jer je najlakši i pripisao mu je atomsku masu 1 [2], sugerirajući da su svi elementi sastavljeni od sitnih, neuništivih čestica, zvanih atomi, koji su svi jednaki i imaju istu masu. Atomi nekog elementa mogu pri kemijskoj reakciji ući u sastav kemijskog spoja ili iz njih izaći, ali njihova ukupna masa u sustavu ostaje nepromijenjena. Dalton je pretpostavio da je vodik najlakši element pa je uveo pojam relativne atomske mase (Ar) kao omjer mase atoma elementa i mase atoma vodika. Također je proučavao sljepoću na boje (daltonizam).[3]
Doprinosi
Atomska teorija
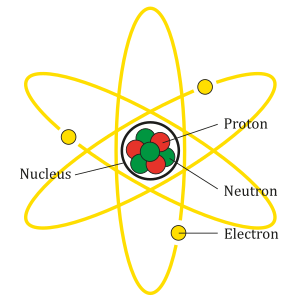
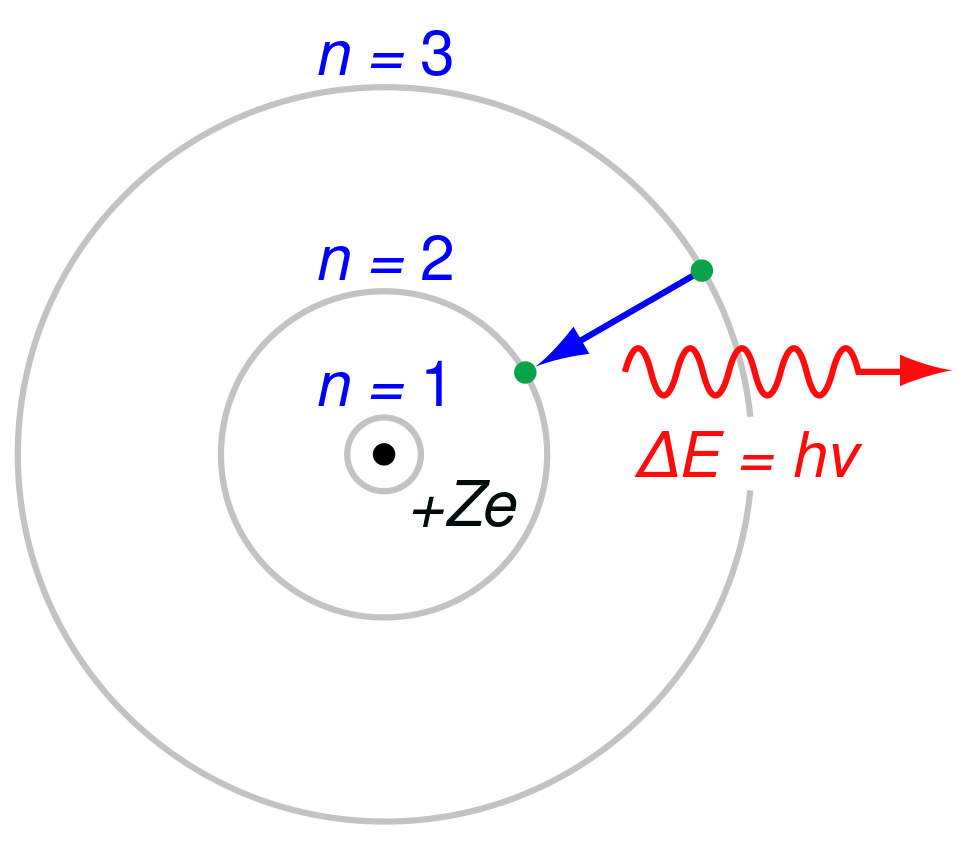
U atomskoj teoriji materije, atom se sastoji od atomske jezgre oko koje kruže elektroni. Danas je općenito priznato mišljenje da se atomska jezgra svih kemijskih elemenata sastoji od pozitivno nabijenih protona i neutrona koji nemaju električni naboj. Čestice koje se nalaze u atomskoj jezgri, to jest protoni i neutroni, zovu se zajedničkim imenom nukleoni (lat. nucleus: jezgra). Neutron ima masu gotovo jednaku masi protona. Proton je jezgra vodikovog atoma, pa mu je masa jednaka masi atoma vodika. Broj protona u atomskoj jezgri koji se zove atomski broj, jednak je njezinom električnom naboju i uvijek odgovara rednom broju kemijskog elementa u periodnom sustavu. Dakle atomskim brojem određena je vrsta kemijskog elementa.
U neutralnom atomu broj elektrona što kruže oko jezgre jednak je broju protona u jezgri. Pozitivan naboj jednog protona jednako je velik kao negativan naboj elektrona. 1869. ruski kemičar D. I. Mendeljejev otkrio je zakonitost ponavljanja kemijskih svojstva elemenata kod povećanja njihove atomske mase. On je tada sve poznate elemente poredao po rastućim atomskim masama jedan iznad drugoga i sastavio periodičku tablicu. Mendeljejev je dokazao da svaki kemijski element ima određen sastav atoma koji označuje atomska masa i mjesto u periodnom sustavu elemenata.
Broj protona P i neutrona N u jezgri određuje atomsku masu A određenog elementa, to jest:
i zove se maseni broj atoma. Na primjer jezgra helija sastoji se od dva protona i dva neutrona. Prema tome je električni naboj jezgre i redni broj helija 2, a relativna atomska masa 4. Oko atomske jezgre kruže negativno nabijeni elektroni, a broj elektrona jednak je broju protona u jezgri.
No kod istog broja protona u jezgri mogu postojati različite količine neutrona. Dva atoma koji imaju isti broj protona, a različiti broj neutrona, imaju skoro ista kemijska svojstva i isti redni broj, ali različite atomske mase. Takvi se elementi koji imaju isti redni broj, a različitu atomsku masu, zovu izotopi. Tako na primjer postoji klor koji ima redni broj 17, to jest njegova jezgra sadrži 17 protona, dok mu je atomska masa 35, što znači da jezgra njegova atoma sadrži 18 neutrona (17 + 18 = 35). Međutim, postoji i klor s atomskom masom 37, to jest jezgra njegova atoma sadrži 20 neutrona (17 + 20 = 37). Običan klor koji se nalazi u spojevima u prirodi ima atomsku masu 35,46, što znači da je on smjesa tih dvaju izotopa koji su u njemu zastupani u omjeru 3 : 1, to jest:
Prvi izotop klora pišemo simbolički 17Cl35, a drugi 17Cl37. Gornji broj uz kemijski simbol elementa znači relativnu atomsku masu tog elementa, a donji - broj protona u jezgri tog elementa, odnosno njegov redni broj. I vodik ima svoje izotope: 1H1 obični vodik, 1H2 teški vodik ili deuterij i 1H3 tricij.
Ovakvi izotopi nađeni su gotovo kod svih kemijskih elemenata. Tako uranij, koji je najvažniji u dobivanju nuklearne energije, ima 5 izotopa. Uranij ima redni broj 92, a njegovi izotopi imaju atomske mase 234, 235, 237, 238 i 239. U prirodnom uraniju najjače je zastupljen izotop s atomskom masom 238. Ima ga 137 puta više nego izotopa s atomskom masom 235. Ostalih njegovih izotopa ima još i manje. Izotopi se danas vrlo mnogo primjenjuju u medicini, tehnici i privredi, a naročito su veoma važni u proizvodnji nuklearne energije. Odjeljivanje izotopa vrši se centrifugiranjem, destilacijom, difuzijom i tako dalje.
Da se jezgra atoma koja se sastoji od pozitivno nabijenih protona ne razleti, jer se istoimeni električni naboji međusobno odbijaju, uzrok su privlačne sile koje vladaju, između protona i neutrona. To su takozvane sile jezgre ili osnovne sile koje, iako su vrlo velike, djeluju samo na vrlo male daljine, to jest u dimenzijama atomske jezgre. Tumačenje tih sila spada danas u glavne probleme atomske fizike.[4]
Relativna atomska masa
Relativna atomska masa (oznaka Ar) je svojstvena veličina svakog kemijskog elementa (stariji naziv: atomska težina). To je broj koji pokazuje koliko je puta prosječna masa atoma nekog elementa veća od 1/12 mase atoma ugljikova izotopa 12C, to jest to je omjer između prosječne mase atoma nekog kemijskog elementa i unificirane atomske jedinice mase. Izražavanje atomskih masa relativnim jedinicama uveo je 1803. John Dalton, koji je za mjernu jedinicu uzeo vodikov atom kao najlakši od svih atoma i pridijelio mu vrijednost 1 (poslije je kao jedinica služila i 1/16 mase atoma kisikova izotopa 16O). Takvo je izražavanje uvedeno iz praktičnih razloga, jer su mase atoma izvanredno malene (na primjer masa je vodikova atoma 1,673 · 10−27 kg). Kako se većina kemijskih elemenata u prirodi pojavljuje u obliku smjese svojih izotopa, relativne atomske mase odgovaraju srednjoj vrijednosti relativnih masa atoma prisutnih izotopa, pa zato redovito nisu cijeli brojevi. Mjerna jedinica relativne atomske mase je broj jedan (1).[5]
Daltonov zakon
Daltonov zakon govori o tlakovima pojedinih vrsta plinova u smjesi plinova, a glasi:
Parcijalni tlak određenog plina u smjesi, je onaj tlak koji bi taj plin imao kada bi sam zauzimao obujam, koji zauzima smjesa. Daltonov zakon nam omogućava odredivanje parcijalnih tlakova plinova prisutnih u atmosferi, poznavanjem njihovih udjela u atmosferskom zraku. Tako, ako je kisik prisutan u zraku udjelom od 21%, tada će i njegov parcijalni tlak biti 21% od ukupnog tlaka zraka.
Matematički, Daltonov zakon se može pisati:
- ili
Gdje p1, p2, ...., pn – prestavlja parcijalne tlakove pojedinih sastojaka smjese plinova. Pretpostavlja se da plinovi ne reagiraju kemijski međusobno:
gdje je pi – parcijalni tlak pojedinog plina, yi – udio pojedinog plina u smjesi.
Daltonov zakon ne opisuje u potpunosti realne plinove. Razlike su pogotovo velike kod visokih tlakova, kada su molekule vrlo blizu jedne drugima, pa dolaze do izražaja međumolekularne sile, i mijenjaju vrijednost tlaka.
Daltonizam
Daltonizam je sljepoća za boje, potpuna ili djelomična nemogućnost raspoznavanja boja. U mrežnici postoje tri vrste receptora (osjetne stanice) za boje (za crvenu, zelenu i plavu boju, a ostale boje nastaju miješanjem tih osnovnih), od kojih svaki sadrži pigment osjetljiv na određenu valnu duljinu svjetlosti. Osoba s normalnim raspoznavanjem boje (trikromat) ima sva tri pigmenta u pravilnim omjerima, dikromati razlikuju samo dvije temeljne boje (obično zamjenjuju crvenu boju zelenom), a monokromati uopće ne razlikuju boje. Daltonizam je najčešće urođen (8% muškaraca i 1% žena) i nedostupan je liječenju.
Izvori
- ↑ Dalton, John, [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2018.
- ↑ Filipović, Lipanović: "Opća i anorganska kemija", 9. izd., Školska knjiga, Zagreb, 1995., ISBN 953-0-30907-4, str.36.
- ↑ Claus Bernet: John Dalton (1766. - 1844.), Biographisches-bibliographisches Kirchenlexikon, 31, 2010., 309.-332.
- ↑ Velimir Kruz: "Tehnička fizika za tehničke škole", "Školska knjiga" Zagreb, 1969.
- ↑ relativna atomska masa, [2] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2018.




