Srebrov nitrat
| Srebrov nitrat | |

| |
| Strukturna formula | |
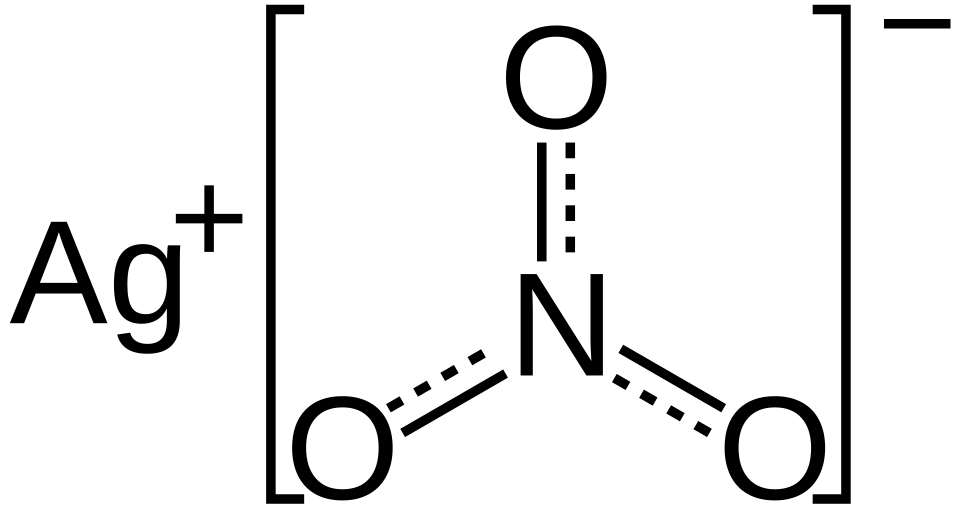
| |
| Svojstva | |
| Sistemsko ime | Srebrov nitrat |
| Molekulska formula | AgNO3 |
| Molarna masa | 169,87 g/mol (bezvodni) 404,00 g/mol (nonahidrat) |
| Izgled | bijeli kristali |
| CAS broj | 7761-88-8 |
| Gustoća | 4,35 g/L (bezvodni) |
| Topljivost u vodi | vrlo topljiv (2,16 kg/L pri 20 °C) |
| Talište | 212 °C |
| Vrelište | 444 °C (razgradnja) |
Srebrov nitrat (srebrov(I) nitrat) je sol srebra kemijske formule AgNO3. Zbog svoje velike topljivosti u vodi i drugim polarnim otapalima, puno manje osjetljivosti na svjetlost od srebrovih halida, kao i niže cijene zbog manjih troškova proizvodnje, koristi se kao univerzalni prekursor za sintezu mnogih drugih spojeva srebra.
Svojstva
Srebrov nitrat kristalna je tvar bijele boje. Talište mu je pri 212 °C, a vrelište pri 444 °C uz razgradnju na elementarno srebro, dušikov(IV) oksid i kisik
- 2AgNO3 → 2Ag + O2↑ + 2NO2↑
Relativno je stabilan na svjetlost. Dobro se otapa u vodi i drugim otapalima. Nije higroskopan, za razliku od npr. srebrovog fluoroborata ili perklorata.
Sinteza
Srebrov nitrat može se jednostavno pripraviti reakcijom metalnog srebra s dušičnom kiselinom:
- Ag + 2HNO3 → AgNO3 + NO2↑ + H2O
Reakciju je potrebno izvoditi u digestoru zbog razvijanja dušikovih oksida[1].
Uporaba
Prekursor za sintezu drugih spojeva srebra
Pri izradi fotografskog filma otopina srebrovog nitrata se miješa s otopinom halidne soli natrija ili kalija čime nastaje netopljivi srebrov halid in situ u fotografskom gelu koji se nanosi na vrpce od tri-acetata ili poliestera.
Srebrov nitrat se također koristi za pripravu nekih eksploziva kao što su srebrov fulminat, srebrov azid i srebrov acetilid.
Reakcija srebrovog nitrata s lužinom daje tamno sivi srebrov oksid:
- 2AgNO3 + 2NaOH → Ag2O + 2NaNO3 + H2O
Odvajanje halidnih aniona
Kation srebra, Ag+, brzo i ireverzibilno reagira s halidnim anionima čime nastaje netopljivi srebrov halid, koji je obično kremasti talog. Ova se reakcija uobičajeno koristi u anorganskoj i analitičkoj kemiji kod odvajanja halidnih aniona:
- Ag+ (aq) + X− (aq) → AgX (s)
Izvori
- ↑ Priprava srebrovog nitrata http://www.youtube.com/watch?v=d6hPgGV_qAg&feature=channel_page